Что касается планирования хирургического лечения ЭД, связанной с МВ, с помощью фаллопротеза, важно классифицировать МВ в зависимости от его расположения и протяженности. В этом контексте мы классифицируем МВ на:
Кавернома головного мозга. Что это
Точных статистических данных о распространенности МВ нет; считается, что он встречается примерно у 0,5% населения Земли. Многие люди могут прожить жизнь, никогда не замечая каверномы (проявления болезни).
Большинство церебральных каверном возникают в большом мозговом сегменте над мозжечком (суправентрикулярные). Это кавернозные полости, которые выглядят как венозные сосуды, наполненные кровью. Однако убедительного прямого кровоснабжения нет, т.е. питающие сосуды не видны при ангиографии. Кавеолы проявляются кровоизлияниями, хотя, как уже говорилось, они не имеют надежного кровоснабжения, или приступами, которые могут быть очень разнообразными (вплоть до эпизодов помешательства, бегства, экстаза, как в случае с этим пациентом). В большинстве случаев кавернозные припадки возникают поодиночке, но они могут быть множественными и обычно являются частью генетического, наследственного заболевания. Эти гемангиомы нельзя удалить открытым хирургическим путем. Каверномы ствола мозга занимают особое положение и могут иметь очень серьезные последствия для здоровья, если они разрываются и кровоточат. Существуют также каверномы спинного мозга.
Лечение каверномы головного мозга
Единого метода лечения каверномы головного мозга не существует. Каверномы, которые связаны с эпилепсией или кровотечением и доступны, должны быть удалены хирургическим путем. Каверномы ствола мозга также оперируются некоторыми нейрохирургами, но эта процедура требует большой материально-технической инфраструктуры, нейрофизиологического мониторинга и большого хирургического мужества и мастерства.
Вопрос о применении радиохирургии (Гамма-нож) в лечении sinus cavernosus остается открытым, доказательств ее эффективности нет.
Пример удаления каверномы передних отделов правой височной доли головного мозга
Пациент мужского пола, 1989 года рождения, поступил в PHCB со сложными припадками.
МРТ головного мозга показала наличие небольшого кавернозного синуса в правой височной доле мозга, до 1,5-2 см в диаметре.
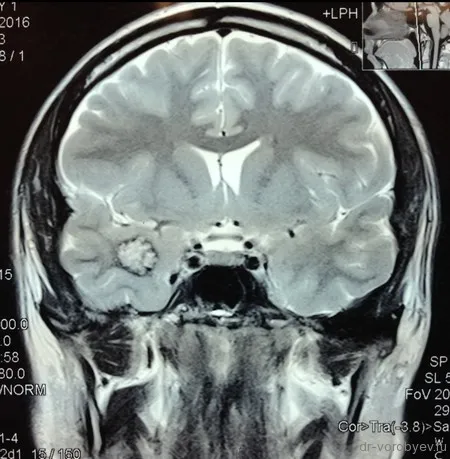
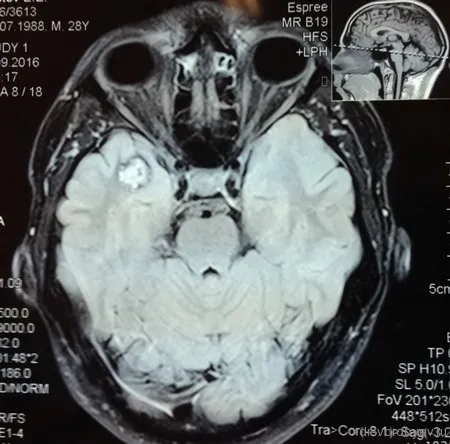
Основные причины болезни
Точная причина патологии пока не ясна. Медицинские эксперты считают, что полость является врожденным состоянием, вызванным вирусной инфекцией в матке во время формирования плодного кровообращения. К факторам, которые также могут привести к развитию сосудистых мальформаций у ребенка, относятся:
- позднюю беременность;
- хронические болезни в организме матери;
- травмы во время родов;
- вредные привычки матери.
Нельзя исключить развитие каверномы на другом этапе жизни. Причины возникновения опухоли могут быть следующими:
- черепно-мозговые травмы;
- лучевая терапия;
- инфекции;
- слабый иммунитет;
- воспаления мозга;
- наследственность.
В некоторых случаях кавернома мозжечка вызывается ангиомами, гемангиомами и другими опухолями головного или спинного мозга.
Разновидности недуга
Типы патологии различают в зависимости от того, где располагается доброкачественное образование: лобная (правая лобная) или теменная, левая височная, мозжечковая и тромботическая ангиома.
Гистологически можно выделить три типа каверном:
1. 1. Классический сорт — самый распространенный. Кавернозно-капсулярная масса без сосудов, волокон и аномалий мозговой ткани, четко отграниченная от мозга.
2. смешанная — за исключением кавернозных опухолей, опухоль состоит из множества сосудов с промежуточными слоями мозговой ткани.
3. пролиферативный — с участками эндотелиальной пролиферации.
Различают также подострый и хронический коллапс, с симптомами, указывающими на кровоизлияние, и без них. Клиническая картина зависит от типа заболевания. Лечение различных типов каверномы также может быть различным. Наши современные диагностические возможности позволяют поставить наиболее точный диагноз и назначить правильное лечение таких опасных состояний, как кавус, остеохондроз шейного отдела позвоночника, грыжа межпозвоночного диска и др.
Какую опасность представляет патология
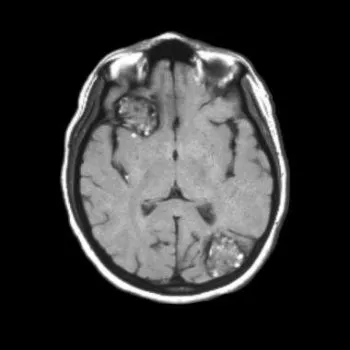
Последствия каверномы зависят от места ее расположения. Помимо головных болей, спазмов, тошноты и рвоты, опухоль может сопровождаться психологическими нарушениями (неспособность нормально воспринимать окружающее, потеря практических навыков, отсутствие самокритики). В результате заболевания могут возникнуть потеря речевой функции и слуховые галлюцинации. Во многих случаях возникают нарушения глотания, судороги и разрывы сосудов. Особенно опасны кровотечение, недостаток кислорода к мозгу и паралич.
Наиболее опасны последствия кавернозного синуса в доминантной височной доле. Смерть наступает при поражении дыхательной или вазомоторной систем.
Патогенез
Прогрессирование любой формы туберкулеза легких может привести к дезинтеграции легочной ткани с дальнейшей кавитацией. К факторам, влияющим на этот процесс, относятся снижение общей и иммунной резистентности на фоне дополнительной сенсибилизации, возникновение различных заболеваний, массовая переинфекция и лекарственная устойчивость микобактерий.
Повышенная секреция связана с такими процессами, как иммунная дисфункция и обязательное увеличение популяции бактерий. Происходят нарушения микроциркуляции и разрушается система сурфактантов. Из поврежденных клеточных элементов формируются кистозные массы, которые заполняют альвеолы. Лейкоциты выделяют протеолитические ферменты, которые расплавляют кистозные массы и частично поглощаются (реабсорбируются) макрофагами. Желчные массы изгоняются через дренажную петлю, и образуется легочная полость распада. В других случаях деструктивный процесс может начинаться с поражения бронхов и панбронхита, с последующим разрушением прилегающей легочной ткани и образованием бронхогенной полости распада. Другой путь формирования бронхогенной полости — проникновение возбудителя в уже сформировавшийся бронхоэктаз.
Полость кариеса окружена широким слоем жевательных, некротических масс. Внешне они граничат с туберкулезными гранулемами, состоящими в основном из гигантских и эпителиоидных клеток. В наружной части грануляционного слоя постепенно формируются коллагеновые волокна, образуя тонкий волокнистый слой с нерегулярной структурой. В результате вокруг полости образуется трехслойная стенка, характерная для полости.
Внутренний слой сформированной стенки состоит из жевательных, некротических масс. Средний слой состоит из грануляционной ткани. Наружный слой состоит из концентрически расположенных волокон. Формирование стенки полости занимает 2-4 месяца. Бывают исключения, когда казино-некротические образования выходят из инкапсулированного очага (туберкулез). В таких случаях образуется полость с трехслойной стенкой, в которой уже присутствует ранее сформированный волокнистый слой.
Ранняя (свежая) полость всегда круглая или овальная. Он окружен легочной тканью, которая мало изменена и не имеет значительных фиброзных или воспалительных изменений. Такие полости образуются при кавернозном туберкулезе.
В зависимости от природы и типа механизма, полости образуются в :
- секвестрирующие
- протеолитические
- атероматозные
- альтеративные
Говорят, что протеолитическая полость расплавляется в центре легочного очага и постепенно распространяется к периферии. Изолирующая полость образуется, когда известковые массы плавятся по краям и распространяются к центру. По мере расплавления сыровидных масс в инкапсулированных очагах образуются атеросклеротические полости. В некоторых случаях ухудшение состояния приводит к нарушению микроциркуляции и питания тканей в области туберкулезного поражения с последующим некрозом отдельных зон. В этом случае говорят об образовании альтернативной формы кавитации.
При образовании полостей туберкулезный процесс чаще всего распространяется на слизистую оболочку дренирующего бронха. Просвет сужается туберкулезными гранулами, затрудняя выход воздуха из полости. В результате объем полости может увеличиться во много раз, и полость, как говорят, «расширяется». Ухудшение бронхиального дренажа затрудняет опорожнение («выход») содержимого полости, усиливает воспалительную реакцию и общую интоксикацию.
Симптомы
Полостной туберкулез легких чаще развивается вследствие безуспешного лечения других форм туберкулеза. Пациенты могут жаловаться на кашель с небольшим количеством слизисто-гнойной мокроты. Иногда может наблюдаться потеря аппетита, повышенная утомляемость и перепады настроения. Эти жалобы могут быть вызваны высокими дозами или длительным приемом лекарств. При недавно диагностированном кавернозном туберкулезе жалобы в большинстве случаев отсутствуют.
При перкуссии грудной клетки над кавернозной областью слышен короткий перкуторный звук из-за уплотнения плевральной и легочной тканей вокруг кавернозного синуса. Пациента просят откашляться и глубоко вдохнуть, после чего над пораженной областью выслушиваются отдельные влажные и сухие хрипы. У большинства пациентов кариозные полости «немые», то есть их нельзя обнаружить при физическом осмотре.
При туберкулезе фибро-абдоминальной области возникают такие симптомы:
- кашель с мокротой
- проявления интоксикации
- кашель продуктивный
- примеси крови в мокроте (иногда)
- одышка
- смещение органов средостения в сторону поражения
- деформированная грудная клетка
- выраженная и разнообразная стетоакустическая симптоматика
Тяжесть симптомов варьируется в зависимости от фазы туберкулезного процесса. Как уже говорилось, болезнь принимает волнообразный характер. Во время обострения у пациента много жалоб. Состояние становится удовлетворительным с короткими ремиссиями. При правильном лечении этой формы легочного туберкулеза поражения в большинстве случаев регрессируют, и состояние стабилизируется. Длительное лечение уменьшает воспаление перибронхиальной области, частично устраняет грануляционный слой и рассасывает туберкулезные очаги. Такая динамика характерна для ограниченного фиброзно-кишечного туберкулеза.
Рентгенологическая картина при кавернозном и фиброзно-кавернозном туберкулезе легких
Рентгенологическое исследование выявляет туберкулезные полости в верхней части легкого, которые являются полостями распада при многих клинических формах заболевания, за которыми следует полостной туберкулез. Компьютерная томография обычно используется для диагностики кавернозной полости и ее динамики и считается наиболее информативным методом в этих случаях.
В большинстве случаев кавернозного туберкулеза обнаруживается одиночная округлая полость диаметром 4 см или менее. Толщина стенки каверны составляет 2-3 мм. Внутренний контур стенки четкий, а наружный часто нечеткий и неровный, особенно при наличии периферического воспаления. Когда полости образуются вследствие очагового туберкулеза или ТБ, изменения в окружающей легочной ткани называют мягкими. Тени фиброзных рубцов и очагов часто обнаруживаются вокруг полостей, развивающихся при инфильтративном или диффузном туберкулезе легких. Рубцовая полость не имеет нормальной формы.
При фиброзно-кавернозной форме рентгенологические данные могут варьироваться в зависимости от начальной формы заболевания, длительности туберкулеза, распространения патологического процесса и т.д. Отмечаются одна или 2-4 кольцевидные тени, мультиморфные очаговые тени инфильтрации бронхов и фиброзное сморщивание пораженных участков легкого. Кольцевые тени могут иметь минимальный диаметр 2-4 см и максимальный диаметр, равный размеру доли легкого. Форма обычно полициклическая или неправильная и очень редко может быть круглой. Внутренний контур стенки каверны отчетливый.
Лечение
Диета № 11
Лечение: В зависимости от давности заболевания, пациентов с фиброзно-кавернозным туберкулезом легких без множественной лекарственной устойчивости лечат по схеме DOTS 1 и 2 с интенсивной фазой химиотерапии, проводимой в стационаре.
Вновь диагностированные пациенты с фиброзно-кавернозным туберкулезом легких получают лечение в соответствии с DOTS 1: В интенсивной фазе назначаются четыре основных противотуберкулезных препарата: изониазид 0,3, рифампицин 0,45-0,6, пиразинамид 1,5-2,0 и стрептомицин 0,5-1,0 или этамбутол 0,8-1,2 в течение 2-4 месяцев, в зависимости от прекращения бактериальной экссудации, в зависимости от веса пациента.
У пациентов с рецидивирующим фиброзирующим туберкулезом, у пациентов, не прошедших предыдущие циклы химиотерапии, при прекращении лечения, а также у хронических пациентов, не получивших ранее полный цикл химиотерапии, лечение проводится по схеме DOTS 2, т.е. в интенсивной фазе назначается 5 основных препаратов с учетом веса пациента: Изониазид 0,3, рифампицин 0,45-0,6, пиразинамид 1,5-2,0, этамбутол 0,8-1,2 и стрептомицин 0,5-0,75 в течение 3-5 месяцев до достижения стабильной конверсии мазка. Параллельно с химиотерапией назначаются витамины, дезинтоксикационные средства, гепатотропные препараты, антиоксиданты и симптоматическая терапия.
Лечение коллапса заключается во введении воздуха в грудную полость (искусственный пневмоторакс, ИП) или в брюшную полость (искусственный пневмоперитонеум).
Показания к коллапсотерапии: 1. ограниченные деструктивные формы туберкулеза легких, когда нет закрытия полости или убедительной положительной динамики после 2-3 месяцев химиотерапии. 2. воздух в грудную или брюшную полость вводится при срочных показаниях в случае легочного кровотечения.
Коллапсотерапия противопоказана при некоторых поражениях бронхов и при прогрессирующем течении фиброзно-кавернозного туберкулеза легких.
Список основных препаратов: 1. *Изониазид+рифампицин+пиразинамид таблетки 60 мг+30 мг+150 мг; 150 мг+75 мг+400 мг; 150 мг+150 мг+500 мг (для интермиттирующего лечения три раза в неделю) 2. *Стрептомицин порошок для приготовления 1 000 мг раствора для инъекций 3. *Этамбутол таблетки 200 мг, 400 мг
Список дополнительных лекарственных средств: 1. *Раствор цианокобаламина для инъекций в ампуле 1 мл (500 мкг) 3. *Раствор тиамина 5% для инъекций в ампуле 1 мл 4. *Раствор аскорбиновой кислоты для инъекций 5%, 10% в ампуле 2 мл, 5 мл 5. *Декстроза д/и 5% 10% раствор фл 400 мл, 500 мл 6. *Натрия хлорид, раствор д/и фл д/крови везам 200 мл 7. *Декстран раствор для инфузий во флаконе 200 мл, 400 мл 8. *Альбумин раствор для инфузий в ампулах 5%, 10%, 20% 9. Этамзилат 250мг, ампула. 10. *Аминокапроновая кислота, раствор 5% раствор-100 мл 11. *Цефазолин порошок для приготовления раствора для инъекций 1000 мг 12. *Цефтриаксон порошок для приготовления раствора для инъекций 250 мг, 500 мг, 1. 000 мг в ампулах 13. *Флуконазол 50 мг, 150 мг капсулы; раствор в ампуле 100 мл для внутривенного введения 14. *Нистатин, 500 000 МЕ, таблетки 15. *Интраканозол пероральный раствор 10 мг/мл, капсулы 100 мг. 16. *Адеметионин 400 мг, сублимированные таблетки, порошок для приготовления 400 мг раствора для инъекций 17. *Урсодеоксихолевая кислота таблетки 250 мг 18. *Селимарин, капсулы. 19. *Гидрокортизона ацетат, ампула. 20. *Преднизолон, таблетки 5 мг 21. *Преднизолон, раствор для инъекций 30 мг/мл 22. *Глюконат кальция 10% препарат 10 мл 23. *Хлорид кальция 10% фл 200 мл 24. *Хлоропирамин 25 мг, таблетки 25. *Атенолол 50 мг, 100 мг, табл. 26. *Эналаприл 2,5 мг, 10 мг, табл. 27. *Ацетилсалициловая кислота, таблетки 500 мг 28. *Парацетамол 200 мг, 500 мг, таблетки 29. *Диклофенак натрия 25 мг, 100 мг, 150 мг таблетки, 75 мг/3 мл раствора для инъекций.
Показания к операции
Удаление кавернозного синуса является признанным эффективным методом лечения этого заболевания. В то же время установление показаний к операции является сложной задачей. В основном это связано с тем, что заболевание обычно имеет доброкачественное течение. У подавляющего большинства пациентов на момент лечения отсутствуют объективные симптомы поражения ЦНС, а случаи стойкой инвалидности возникают в основном при рецидивирующих кровоизлияниях из глубоких кавернозных структур и ствола мозга, к которым трудно получить хирургический доступ. С другой стороны, невозможно предсказать течение болезни в каждом отдельном случае, а успешная операция может навсегда избавить пациента от рисков, связанных с болезнью. Мы считаем, что расположение кавернозного синуса и клиническое течение заболевания являются основными критериями показаний к операции. Исходя из этих факторов, хирургическое вмешательство показано в следующих случаях.
Поверхностные кавеолы вне функционально значимых зон, проявляющиеся кровотечением или судорогами,
корковые и подкорковые каверномы в функционально значимых областях, глубокие каверномы больших полушарий, каверномы ствола мозга и каверномы средних полушарий мозжечка, характеризующиеся рецидивирующими кровоизлияниями и стойким неврологическим дефицитом или тяжелой эпилепсией.
Помимо этих критериев, существуют определенные условия, определяющие показания к операции: размер полости, возраст пациента, сопутствующие заболевания и другие. Во всех случаях показания к удалению кавернозного тела являются относительными, поэтому обязательным условием для принятия решения является знание пациентом характера и течения заболевания, цели операции и ее возможных последствий. Радиохирургия является одним из вариантов лечения труднодоступных каверном, хотя ее эффективность спорна. Пациент должен быть проинформирован о риске осложнений при использовании этой техники.
Хирургические вмешательства: техника и результаты
Планирование доступа и хирургические процедуры при удалении полостей полушарий в целом соответствуют общим принципам, используемым в хирургии опухолей головного мозга. В случае поверхностной подкорковой локализации поиск порока развития значительно облегчается наличием постгеморрагических изменений в поверхностной коре и мозговых оболочках. Кавернома обычно четко отграничена от продолговатого мозга, что облегчает ее выделение. В случае локализации каверномы вне функционально важных зон, выделение дисплазии с периферическими изменениями и ее удаление одним блоком значительно облегчает и ускоряет операцию. В некоторых случаях для улучшения результатов лечения эпилепсии используется также удаление вещества мозга, макроскопически измененного продуктами распада крови вокруг кавернозного синуса, хотя эффективность этого метода спорна. Хирургическое удаление кавернозных тел, расположенных в функционально важных корковых и подкорковых областях мозга, а также в глубоких структурах больших полушарий, имеет некоторые особенности. В случае кровотечения из полостей такого типа пациент должен находиться под наблюдением еще 2-3 недели. Отсутствие регресса очаговых симптомов в этот период является дополнительным основанием для проведения операции. Решение об операции не следует принимать до тех пор, пока гематома не рассосется, так как инструментарий и гель делают процедуру более травматичной. Внутренняя декомпрессия кавеол с удалением гематомы является необходимым шагом при удалении кавеол из функционально важных областей, так как это уменьшает хирургическую травму. Резекция периапикальных постгеморрагических изменений не показана.
Удаление небольшой полости с помощью нейропластики
Для улучшения результатов удаления полости используются различные методы интраоперационной поддержки. При отсутствии четких анатомических ориентиров полезны методы интраоперационной навигации. Ультрасонография позволяет визуализировать полость и спланировать маршрут доступа в большинстве случаев. Важным преимуществом метода является предоставление информации в режиме реального времени. Ультразвуковое исследование полостей может быть затруднено при небольших поражениях. Бескаркасное нейропланирование, основанное на данных предоперационной МРТ, позволяет планировать необходимый доступ (как можно меньший для данной ситуации) и краниотомию с максимально возможной точностью. Этот метод подходит для поиска небольших полостей. Стимуляция моторной зоны с оценкой моторных ответов и М-ответов должна использоваться во всех случаях возможного интраоперационного повреждения моторной коры или пирамидных трактов. Эта техника может быть использована для планирования максимально щадящего подхода к кавернозному синусу и оценки возможности рассечения перикортикальной области вещества мозга. Интраоперационное использование ЭКГ для оценки необходимости резекции отдаленных очагов эпилептиформной активности целесообразно у пациентов с длительным анамнезом эпилепсии и припадками, устойчивыми к лекарственным препаратам. ЭКГ-направленная тонзиллэктомия была особенно эффективна при эпилептических поражениях средних височных структур. Полное удаление дисплазии должно быть предпринято во всех местах расположения кавернозных тел, так как частично удаленные кавернозные тела часто рецидивируют. Венозные ангиомы в непосредственной близости от кавернозного синуса должны быть сохранены, поскольку их резекция связана с развитием венозного дренажа из соседнего вещества мозга. В большинстве случаев кавеомы удается полностью удалить, даже если они очень большие, и результат операции обычно хороший: у большинства пациентов нет неврологических нарушений. Состояние пациентов с припадками улучшается в 75% случаев, а в 62% случаев припадки больше не возникают после удаления кавернозного синуса. Риск послеоперационных неврологических осложнений во многом зависит от расположения образования. Частота поражения кавеол, расположенных в функционально несмежных частях больших полушарий, составляет 3 %. Для кортикальных и субкортикальных кавеол в функционально важных областях этот показатель увеличивается до 11%. Риск развития или усугубления неврологического дефицита при удалении глубоких полостей составляет 50%. Следует отметить, что послеоперационный неврологический дефицит часто обратим. Послеоперационная смертность составляет 0,5 %.
Каверномы ствола головного мозга
Лечение кавернозных ангиом ствола головного мозга имеет ряд особенностей, которые оправдывают выделение этой патологии в отдельную группу. Во-первых, анатомия и функциональная важность ствола мозга делают хирургические вмешательства в этой области чрезвычайно сложными. Из-за компактного расположения большого количества различных структур, в том числе жизненно важных, в стволе мозга, любое кровотечение из corpora cavernosa, каким бы малым оно ни было, приводит к неврологическим нарушениям, что отличает течение заболевания от клинических проявлений в corpora cavernosa больших полушарий. Небольшой размер стволовых полостей часто затрудняет гистологическую верификацию патологии, поэтому характер заболевания чаще остается незамеченным, чем при полостях в других местах. По данным МРТ и хирургии можно выделить три варианта патологических образований, которые объединены под общим названием «стволовые кавеомы»: — подострые и хронические гематомы, при удалении которых ткань кавернозного тела обнаруживается только в 15% случаев. Нельзя исключить, что эти гематомы обусловлены не полостями, а другими пороками развития, возможно, телеангиэктазией;- типичные полости, связанные с острыми, подострыми или хроническими гематомами;- типичные гетерогенные полости, окруженные кольцом гемосидерина, без признаков кровоизлияния.В клиническом течении туннельных полостей существует два основных варианта. Инсультоподобный вариант характеризуется острым развитием тяжелых стволовых симптомов, часто сопровождающихся сильной головной болью. Этот вариант обычно наблюдается при гематомах в области туловища без признаков МРТ кавернозного синуса. Псевдотуморный вариант характеризуется медленным прогрессированием стволовых симптомов, иногда продолжающимся до нескольких месяцев. Этот курс характерен для пациентов с типичными МРТ-изображениями каверномы. При обоих вариантах течения клинические симптомы постепенно стабилизируются, а затем могут полностью или частично регрессировать. Анализ результатов хирургического вмешательства показал, что они четко зависят от типа обнаруженного образования. Например, удаление подострых и хронических стволовых кровоизлияний приводило к исчезновению симптомов в 80% и 60% случаев соответственно. Когда удалялись полости с признаками кровотечения, клинические результаты были менее удовлетворительными, а когда удалялись полости без признаков кровотечения, результаты обычно были неудовлетворительными. Выявление этих закономерностей послужило основой для определения показаний к операции.
Основными показаниями к хирургическому лечению стволовых полостей являются наличие подострого или хронического кровотечения, рецидивирующее кровотечение и постоянно нарастающие симптомы травмы ствола. При магистральной гематоме оптимальное время для вмешательства составляет 2-4 недели с момента кровотечения и образования гематомы. Консервативной операции следует отдавать предпочтение в тех случаях, когда неврологические симптомы значительно разрешились к моменту обращения к врачу, объем гематомы небольшой (менее 3 мл), мальформации глубоко локализованы и поэтому существует высокий риск усиления симптомов после операции.
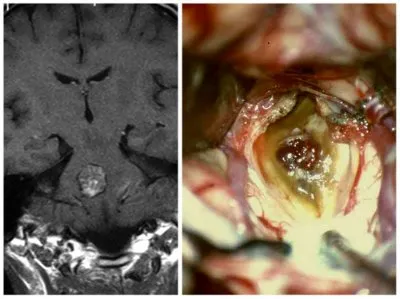 |
| Удаление полости ствола |
Выбор хирургического подхода всегда основывается на тщательном изучении топографии образования с помощью МРТ. Гематома и/или кавернозный синус удаляются со стороны, ближайшей к поверхности ствола мозга. Наиболее часто используется срединно-подключичная краниотомия с доступом через четвертый желудочек. Это связано с тем, что большинство гематом и мальформаций располагаются субэпендимально по отношению к черепу. Даже при больших гематомах, занимающих почти все поперечное измерение ствола, этот подход является наиболее приемлемым по сравнению с другими подходами из-за своей простоты и меньшей травматичности. Для кавернозных тел и гематом, расположенных в вентрально-латеральных отделах моста, мы считаем оптимальными заднелабиальный, переднелабиальный и подслизистый подходы, так как они обеспечивают более широкий обзор операционного поля и, следовательно, больше шансов на радикальное удаление дисплазии и капсулы хронической гематомы. Умеренные церебральные гематомы и мальформации могут быть удалены через субвентрикулярный, суправентрикулярный или субцефалический трансвентрикулярный подход. Важным этапом процедуры является определение проекции расположения ядер NMN в нижней части ромбовидной ямки (картирование) путем записи двигательных ответов. Информация о расположении основных ядер ствола мозга позволяет хирургу оперировать как можно дальше от этих структур. В хирургии ствола мозга не используются шпатели — хирург создает поле зрения с помощью инструментов, используемых для операции — отсоса, щипцов, ножниц и т.д. Во время операции кавернозная ангиома разбивается на фрагменты и удаляется по частям. Если гематома хроническая, капсула должна быть удалена как можно радикальнее. Если кавернозный синус или капсула хронической гематомы удалены не полностью, могут возникнуть рецидивы кровотечения. Чаще всего это происходит после удаления хронических гематом. Это связано с тем, что если стенки гематомы не будут адекватно ревизованы, могут остаться фрагменты небольшой дисплазии, вызвавшей первоначальное кровотечение. Впоследствии эта дисплазия может перерасти в более крупный кавернозный синус.
Симптомы кавернозного туберкулеза легких
Локализация кавернозного туберкулеза легких обычно односторонняя. Заболевание обычно развивается на 3-й или 4-й месяц после неэффективного лечения других форм туберкулеза. Клиническая картина наиболее выражена в фазе распада. Наблюдается кашель с мокротой и кровохарканье. Над полостью разложения выслушиваются влажные хрипы.
После окончания кавитации симптомы мягкие, не очень выраженные и неспецифические. Могут наблюдаться тошнота, постоянная усталость, потеря аппетита, потеря веса и периодическая гипотермическая лихорадка. Пациенты с кавернозным туберкулезом легких являются резервуаром инфекции и источником распространения микобактерий. Поэтому бактериурия часто является основанием для более детального обследования пациента.
Легочное кровотечение, возникающее без причины в здоровом состоянии, может указывать на скрытый туберкулез. Так называемые аневризмы Расмуссена (когда в процесс вовлекаются терминальные легочные артерии), аспергиллез полостей, включая рассекающие полости, могут быть причиной сильного кровотечения. Осложненное течение полостного туберкулеза также включает разрыв кавернозного синуса в плевральной полости с развитием бронхолегочного свища или плеврального инфаркта.
Полостной туберкулез легких длится не более 2 лет. Заживление кариозных полостей может принимать различные формы: Рубец, туберкулез, изолированное туберкулезное поражение или дезинфицированная полость. В других случаях полостной туберкулез перерастает в фиброзирующий полостной туберкулез легких.
Диагностика
При выявлении полостного туберкулеза легких пациенты обычно уже состоят на учете у флеболога и имеют в анамнезе туберкулезные инфекции. В редких случаях туберкулез впервые обнаруживается на этой стадии, обычно во время рентгеновского обследования. Акустические результаты неинформативны, поэтому кариес часто называют «немым». Показатели крови часто находятся в пределах нормы, иногда отмечается легкая нейтрофилия, лимфоцитопения и повышенная скорость оседания эритроцитов.
Дальнейшее рентгенологическое исследование (рентген грудной клетки) показывает кольцевидные тени с периферической овальной или круглой локализацией. По результатам рентгенологического исследования необходимо провести дифференциальный диагноз с абсцессом легкого, периферической карциномой легкого, буллезной эмфиземой, ограниченным пневмотораксом, эхинококкозом и дренирующим плевритом.
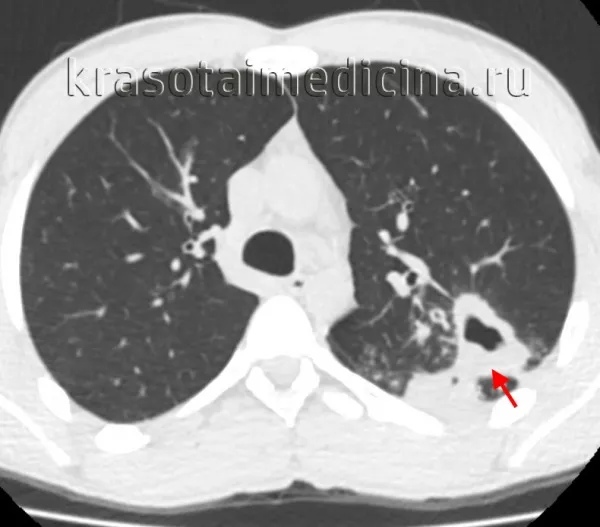
КТ грудной клетки. Кавернозное образование (полость) в задней S3 левой верхней доли легкого.
При первоначальной диагностике полостного туберкулеза легких наблюдается высокая частота положительных результатов исследования мазков. Бронхоскопия необходима не только для получения материала для исследования при отсутствии мокроты, но и для выявления воспалительных изменений в бронхах (эндобронхит), препятствующих бронхиальной обструкции. Результат туберкулиновой пробы слабоположительный. Лабораторные тесты (QuantiFERON-TB, T-SPOT.TB) очень полезны в этих случаях.
Лечение кавернозного туберкулеза
Из-за активного бактериовыделения пациенты с полостным туберкулезом легких должны лечиться как стационарные больные в противотуберкулезной клинике. Лечение вновь диагностированного кавернозного процесса заключается в одновременном приеме 3-4 противотуберкулезных препаратов (обычно изониазида, этамбутола, рифампицина и стрептомицина). Для обеспечения высоких концентраций специфических химиотерапевтических агентов их можно вводить внутривенно, внутрибронхиально или непосредственно в полость тела. Кроме того, назначается туберкулотерапия, лечебная дыхательная гимнастика и физиотерапия (индуктотермия, ультразвук, лазеротерапия). Если существует высокий риск устойчивости микобактерий к препаратам, в схему лечения включаются фторхинолоны и канамицин.
В благоприятных случаях специальное лечение, продолжающееся 4-6 месяцев, приводит к положительным результатам: Размножение бактерий прекращается, полость уменьшается и закрывается. Если в течение вышеуказанного периода не удается достичь заживления полости, принимается решение о хирургическом лечении туберкулеза полости: Резекция легкого, хирургическое лечение коллапса (введение искусственной легочной грудной клетки). В любом случае, после госпитального этапа проводится стационарное и амбулаторное лечение и последующее наблюдение.
Результаты исследования
Врожденный МВ был обнаружен у 2 пациентов (12,5%), а приобретенный МВ — у 15 (87,5%). Причины приобретенного МВ были следующими: Последствия ИКТ — 3 пациента (20%), приапизм и его хирургическое лечение — 3 пациента (20%), инфекция простаты — 3 пациента (20%), внедрение инородных тел в corpora cavernosa — 2 пациента (13,3%), последствия радикальной позадилонной простатэктомии при раннем раке простаты — 2 пациента (13,3%), последствия радиотерапии при раке простаты — 1 пациент (6,65%). Структура пациентов в зависимости от локализации ХПН представлена в таблице 2.
Таблица 2. Локализация ХПН.
| Локализация МВ | Количество пациентов |
| Далекая вершина | 1 |
| Средний | 5 |
| Передний ствол | 2 |
| Средняя вершина | 3 |
| Средний ствол | 2 |
| Всего | 2 |
| Всего пациентов: | 16 |
У 3 пациентов с МВ средней степени тяжести наблюдалась локальная МВ протяженностью менее 1 см. В остальных случаях расширение МВ составляло более 1 см.
Кессоны с гидравлическим управлением были имплантированы у 3 пациентов (Mentor Alpha I — 2 случая, AMS Ambicor — 1 случай), пластиковые кессоны были имплантированы у 13 пациентов (AMS 600M и AMS 650 — 10 случаев, Mentor AcuForm — 3 случая). Во время операции 5 пациентам удалось успешно имплантировать фаллопротезы (гидравлически управляемые фаллопротезы — 3, пластиковые фаллопротезы — 2) и закрыть белую мембрану corpora cavernosa без перерастяжения (1-я группа), несмотря на трудности с открытием corpora cavernosa. У остальных 11 пациентов, несмотря на обширную корпэктомию и удаление рубцовой ткани, оставался серьезный дефект белой мембраны кавернозного тела, потребовавший проведения коропластики. У трех пациентов корпэктомия была выполнена с использованием синтетического материала (группа 2); у остальных 8 пациентов процедура была выполнена с использованием кожного лоскута крайней плоти на питающем стволе tunica dartos (группа 3).
Во время процедуры возникли следующие осложнения:
- Перфорация ножек кавернозных тел — у 2 пациентов (12,5%), из которых 1 случай имел место во 2-й группе и 1 в 3-й
- Перфорация межкавернозной перегородки — у 1 пациента 3-й группы (6,25%)
Оба вида осложнений не требовали специфической хирургической коррекции (ушивание corpus cavernosum или межпредсердной перегородки) и не влияли на качество операции. Во всех случаях фаллопротезы были успешно имплантированы.
Послеоперационное наблюдение варьировалось от 1 до 6 лет (в среднем около 3 лет). За этот период послеоперационные осложнения возникли только во 2-й группе прооперированных пациентов. Из 3 пациентов, перенесших соматопластику синтетическим материалом, у двух в послеоперационном периоде развилась инфекция протеза, потребовавшая удаления фаллопластических протезов. В группах 1 и 3 послеоперационных осложнений не было. Все пациенты удовлетворены результатом процедуры и ведут активную половую жизнь.
Обсуждение результатов и выводы
В изученной нами группе пациентов с ЭД вследствие МВ в половине случаев не удалось закрыть склеральную мембрану над фаллопротезом, даже при использовании узких протезов AMS после дилатации corpora cavernosa, обширной соматотомии и резекции corpora cavernosa. Мы не разделяем мнение некоторых урологов, которые считают, что при «недостаточности» склеры нет необходимости полностью закрывать соматотомию и что часть фаллопротеза может быть прикрыта tunica dartos и кожей пениса. Наша позиция основана на том, что оставление части белочной оболочки открытой может привести к деформации полового члена, особенно во время искусственной эрекции управляемого гидравлического фаллопротеза, что способствует миграции пластикового имплантата и теоретически повышает риск инфекции протеза. В связи с этим мы считаем, что закрытие corpora cavernosa и установка в них фаллопротезов является обязательным. Существующие методы соматопластики имеют некоторые недостатки, которые обобщены в таблице 3.
Таблица 3 Очевидные и предполагаемые недостатки существующих методик соматопластики.
| Техника контурной пластики тела | Недостатки |
| Синтетические легкоплавкие пластмассы (16) | Повышенный риск инфекции протеза |
| Свободная эпидермальная кожа (7) | Втягивание протеза, деформация полового члена Требуется дополнительный разрез |
| Автовен (2) | Ретракция протеза, деформация полового члена Недостаточная прочность протеза, возможная миграция протеза Требуется дополнительный разрез |
| Широкая фасция бедра (3) | Втягивание протеза, деформация полового члена Требуется дополнительный разрез |
| Перфорированная стенка тонкой кишки (15) | Недостаточная прочность протеза, возможная миграция протеза Требуется дополнительный разрез Значительное увеличение операционного времени |
Наша практика подтвердила, что использование синтетических протезов связано с повышенным риском инфицирования протеза. Конечно, соматопластика крайней плоти на ножке, питающей tunica dartos, не лишена недостатков (сложность удаления лоскута, более длительное время операции). Однако при наличии соответствующих навыков эти недостатки можно преодолеть. С другой стороны, этот пластиковый материал достаточно стабилен и не склонен к втягиванию, поскольку кровоснабжение самого пластыря сохраняется. Высокая эффективность снабжения tunica dartos из крайней плоти во время имплантации фаллопротеза у пациентов с ЭД и тяжелым ЦП подтверждается результатами нашего исследования. Однако окончательные выводы можно сделать только после дальнейших наблюдений и в результате настоятельно необходимо провести дальнейшие исследования в этой области, возможно, объединив опыт различных специалистов и учреждений.
К счастью, такие сложные случаи имплантации фаллопротеза, связанные с тяжелым МВ, до недавнего времени были редкостью. Однако глобальная тенденция в структуре пациентов с ЭД, обращающихся к урологу, позволяет предположить, что в скором времени урологи будут лечить все более сложных пациентов с разработкой пероральной терапии ЭД, которая может использоваться различными специалистами. Это предъявляет повышенные требования к хирургической технике имплантации фаллопротеза как наиболее эффективному методу лечения случаев ЭД, не поддающихся консервативной терапии. В настоящее время хирург, занимающийся фаллопротезами, должен быть знаком со всеми аспектами проблемы муковисцидоза и особенностями хирургических методик, включая соматопластику. Эти знания и навыки позволят урологам занять новое, более важное место в иерархии специалистов, оказывающих помощь пациентам с МВ.
Список литературы
- Abolfotouh M.A., al-Helali N.S.: Effect of erectile dysfunction on quality of life. East Mediterr Health J., 2001, Vol. 7, N. 3, pp. 510 — 518.
- Brock G, Nunes L., von Heyden B., Martinez-Pineiro L., Hsu G.L., Lue T.F. Can a venous patch graft be a substitute for the tunica albuginea of the penis? J Urol., 1993, Vol. 150, N. 4, pp. 306 — 309.
- Burnett A.L. Fascia lata in penile reconstructive surgery: a reappraisal of the fascia lata graft. Plast. Reconstr. Surg., 1997, Vol. 99, N. 4, pp.1061 — 1067.
- Carson C.C., Mulcahy J.J., Govier F.F. Efficacy, safety and patient satisfaction outcomes of the AMS 700CX inflatable penile prosthesis: results of a long-term multicenter study. AMS 700CX Study Group. J Urol., 2000 Vol. 164, N. 2, pp. 376 — 380.
- Costa P., Avances C., Wagner L.: Erectile dysfunction: knowledge, wishes and attitudes. Results of a French study of 5.099 men aged 17 to 70. Prog. Urol. 2003, Vol. 13, N 2, pp. 85 — 91.
- De Boer B.J., Bots M.L., Lycklama A. et al.: Erectile dysfunction in primary care: prevalence and patient characteristics. The ENIGMA study.: Int. J. Impot. Res. 2004 Feb 12 (опубликовано в электронном виде до печатной публикации).
- Devine C.J., Horton C.E. Surgical treatment of Peyronie’s disease with a dermal graft. J Urol., 1974, Vol. 111, N. 1, pp. 44 — 49.
- Feldman H.A., Goldstein I., Hatzichristou D.G. et al.: Impotence and it’s medical and psychosocial correlates: results of the Massachusetts Male Aging Study. J. Urol, 1994, Vol. 151, p. 56.
- Hall S.J., Basile G., Bertero E.B., de las Morenas A., Goldstein I. Extensive corporeal fibrosis after penile irradiation. J Urol., 1995, Vol. 153, N 2, pp. 372 — 377.
- Lea A.P., Bryson H.M., Balfour J.A. Intracavernous alprostadil. A review of its pharmacodynamic and pharmacokinetic properties and therapeutic potential in erectile dysfunction. Drugs Aging, 1996, Vol. 8, N 1, pp. 56 — 74.
- Leungwattanakij S., Bivalacqua T.J., Usta M.F., Yang D.Y., Hyun J.S., Champion H.C., Abdel-Mageed A.B., Hellstrom W.J. Cavernous neurotomy causes hypoxia and fibrosis in rat corpus cavernosum. J. Androl., 2003, Vol. 24, N2, pp. 239 — 245.
- Lin J.S., Lin Y.M., Chow N.H., Wang S.T., Sun Y.N.: Novel image analysis of corpus cavernous tissue in impotent men. Urology, 2003, Vol. 55, N 2, pp. 252 — 256.
- Lyngdorf P., Hemmingsen L.: Epidemiology study of erectile dysfunction and it’s risk factors: a practice based study in Denmark. Int. J. Impot. Res. 2004, Feb 19 (опубликовано в электронном виде до печатной публикации).
- McAninch J.W. Reconstruction of extensive urethral strictures: circular fasciocutaneous penile flap. J Urol., 1993, Vol.149, N. 3, pp. 488 — 491.
- Monga M., Cosgrove D., Zupkas P., Jain A., Kasyan A., Wilkes N., Rajasekaran M. Small intestinal submucosa as a tunica albuginea graft material. J Urol., 2002, Vol. 168, N 3, pp. 1215 — 21.
- Montague D., Angermeier К.. Penile prosthesis in the Year 2000. AUA Update series. Lesson 31, Vol. XIX. American Urological Association, 2001
- Montorsi F., Salonia A., Deho F., Briganti A., Rigatti P. The ageing male and erectile dysfunction. World J Urol., 2002, Vol. 20, N 1, pp. 28 — 35.
- Moore T.M, Strauss J.L., Herman S., Donatucci C.F.: Erectile dysfunction in early, middle, and late adulthood: symptom patterns and psychosocial correlates. J Sex Marital Ther., 2003, Vol. 29, N 5, pp. 381 — 399.
- Mulcahy J.J. Long-term experience with salvage of infected penile implants. J Urol., 2000, Vol. 163, N 2, pp. 481- 482.
- Parivar E., Lue T.F.: Priapism. In Male Infertility and sexual Dysfunction. Springler-Verlag, New York, 1997, pp. 401 — 408
- Roumeguere Th., Wespes E., Carpentier Y., Hoffmann P., Schulman C.C. Erectile dysfunction is associated with high prevalence of hiperlipidemia and coronary heart disease risk. Europ. Urol., 2003, Vol. 44, N. 3, pp. 355 — 359
- Sanchez de la Vega J., Amaya Gutierrez J., Alonso Flores J.J., Garcia Perez M.: Erectile dysfunction in those under 40. Etiological and contributing factors.: Arch Esp Urol, 2003, Vol. 56, N 3, pp. 161 — 164.
- Seftel AD.: Erectile dysfunction in the elderly: epidemiology, etiology and approaches to treatment. J Urol. 2003, Vol. 169, N. 6, pp. 1999 — 2007.
- Shiri R, Koskimaki J, Hakama M. et al.: Prevalence and severity of erectile dysfunction in 50 to 75-year-old Finnish men. J Urol., 2003, Vol. 170, N. 6, pp. 2342 — 2344.
- User H.M., Hairston J.H., Zelner D.J., McKenna K.E., McVary K.T. Penile weight and cell subtype specific changes in a post-radical prostatectomy model of erectile dysfunction. J Urol., 2003, Vol. 169, N. 3, pp.1175?.
- Wilson S.K. Pearls, Pitfalls and Perils on penile prosthesis implantation. AUA postgraduate course. AUA Annual Meeting, 1998.
- Wilson S.K. Status of Penile Implants. AUA postgraduate course HO 231 PG. AUA Annual Meeting, 2002.