Мышьяк используется для сплавов свинца при изготовлении пуль, так как капля сплава мышьяка со свинцом при отливке пуль в башне имеет строго сферическую форму, а прочность и твердость свинца значительно увеличивается.
Химический элемент мышьяк, крысиный яд или лекарство
С незапамятных времен вокруг этого элемента, который в прошлом был известен и как сильный яд, и как лекарство, существует множество тайн и загадок. Не случайно мышьяк вызвал не только любопытство травников и целителей, но и интерес ученых.
Ходят слухи, что в средние века, когда холера опустошала города, многие люди умирали не от болезни, а от передозировки мышьяка, который местные лекари прописывали людям в качестве лекарства. Симптомы, описанные очевидцами, были очень похожи на симптомы отравления мышьяком.
Вещество, без которого организм не может обойтись, и в то же время очень опасное для здоровья. Ведь всего 60 мг этого яда убьют человека, а в минимальных дозах он обладает рядом полезных свойств.
Что это такое? Описание элемента и его физических свойств
Элемент таблицы Менделеева имеет официальное название (Arsenicum) или мышьяк, что означает желтая серьга, а русское название, вероятно, связано с тем, что его соединения используются для уничтожения мышей и грызунов. В таблице Менделеева этот химический элемент находится под порядковым номером 33 и обозначается как As.
Мышьяк обычно считается металлоидом, но многие ученые считают его скорее неметаллом. Мышьяк — элемент с очень высокой плотностью, что оказывает сильное влияние на его физические и химические свойства. Его атом имеет 3 свободных электрона и обладает валентностью 3, что определяет его химические свойства.
Он имеет типичный стальной цвет с зеленоватым оттенком, но может быть и желтоватым, а в некоторых разновидностях — черным, хотя в чистом виде встречается редко, поскольку является компонентом свинцовых, медных или серебряных руд.
Самые крупные месторождения этого элемента находятся в Грузии, Средней Азии, Казахстане, Великобритании, США, Канаде и других странах Европы и Азии, а также в некоторых районах России.
Несмотря на высокую токсичность, мышьяк обладает многими важными свойствами, которые используются как в медицине, так и в промышленности. В чистом виде As используется в синтезе полупроводников. Другим важным применением является производство красок: сульфиды этого вещества используются для изготовления красок для живописи и дубления. В химической промышленности используется мышьяковая кислота, которая получается при окислении исходного материала.
Интересные исторические данные
В XIX веке в США и некоторых европейских странах был известен косметический чудо-препарат под названием мышьяк, и все дамы были убеждены, что благодаря ему их кожа выглядит мягкой, а глаза сияют.

Дозировка препарата строго регулировалась, начиная с малых доз и постепенно увеличивая…..
Также описаны моменты использования этого вещества в качестве средства для похудения. Его добавляли в крошечных дозах в таблетки для похудения. К чему это в итоге привело, история умалчивает.
Я нашел в Интернете фотографию газетной вырезки из Нью-Йорка, в которой был рецепт вкусных вафель с мышьяком.

Роль мышьяка для организма человека
Помимо свойств, делающих этот минерал незаменимым для промышленности, он является очень токсичным ядом, но полезным и иногда необходимым для здоровья в микродозах.
На самом деле, As является лишь условно токсичным для человека, так как эффект зависит от дозы. А в минимальных дозах он даже необходим для нормального функционирования человеческого организма.
Таким образом, человек должен потреблять 12 — 15 мкг мышьяка в день, который в основном поступает с пищей и водой и всасывается в желудке и кишечнике. Для нормального функционирования он должен присутствовать в организме в количестве 15 мгм.
Соединения этого вещества обладают свойством быстро всасываться в кровь при приеме с пищей. Однако, помимо этого, до 9 % поглощается через дыхание и около 1 % через кожу.
В кровотоке элемент попадает в печень, где проходит процесс образования метильных групп (метилирование) путем присоединения 3 атомов водорода и одного атома углерода к другой молекуле.
Элемент накапливается не только в печени, но и в легких, тонком кишечнике и коже. Уже через 24 часа часть соединений, до 30 %, выводится с мочой и до 4 % — с калом. Оставшаяся часть выводится через кожу и кишечник вместе с выпавшими волосами и отшелушенными частицами кожи.
Наиболее опасной для здоровья человека является неорганическая форма химиката, которая как раздражает желудок, так и изменяет состав крови, влияя на здоровье легких и кожи. Большие количества могут вызвать рак, бесплодие у женщин и выкидыши. Кроме того, эта форма может повреждать ДНК.
Органическая форма соединений мышьяка менее опасна для здоровья, не приводит к образованию злокачественных клеток и не изменяет ДНК, но может вызывать боли в желудке и кишечнике и расстройства нервной системы.
Наиболее важной биологической функцией мышьяка в организме человека является:
- Регуляция фосфорного и азотного обмена, содействие в сохранении фосфора в организме и его усвоение. Его роль сравнивают с ролью витамина D, без которого усвоение кальция в организме невозможно.
- Без его присутствия не проходят окислительные реакции в энергетических станциях клеток — митохондриях.
- Соединения арсеника активизируют процесс кроветворения и улучшают метаболические процессы в клетках.
- Частично стимулирует рост и развитие ткани костной системы, если его недостаточно в организме, то это отражается на росте детей и их развитии и ведет к резкому снижению концентрации жиров.
Из предполагаемых, но пока не доказанных свойств As ученые отмечают, что он может улучшать ферментные реакции в организме, заменяя фосфор, и что некоторые соединения мышьяка могут снижать активность раковых клеток.
Этот элемент входит в состав природного минерального органического вещества мумиё, которое известно многим и используется в лечебных целях.
Мышьяк до сих пор используется на последней стадии лечения сонной болезни. А минеральная вода, содержащая мышьяк, используется для лечения некоторых заболеваний желудочно-кишечного тракта и анемии.
Важное свойство мышьяка: серьга может действовать как противоядие. Являясь антагонистом селена, фосфора и серы, он способен нейтрализовать отравление любым из этих веществ.
СТРУКТУРА
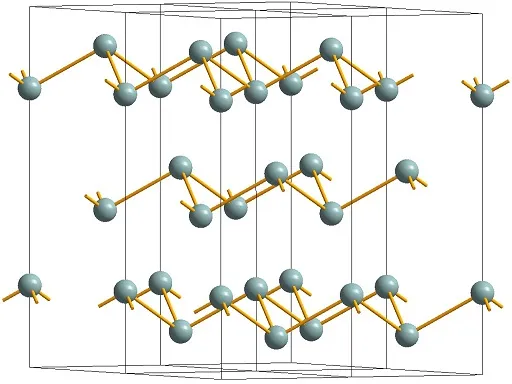
Кристаллическая структура мышьяка представляет собой бидентатную чешуйчатую симметрию. Конвекция треугольная, согласно L633L23PC. Кристаллы чрезвычайно редки и имеют ромбоэдрическую или псевдокубическую форму.
Известно несколько аллотропных модификаций мышьяка. При нормальных условиях металлический или серый мышьяк (альфа-арсенид) стабилен. Кристаллическая решетка серого мышьяка ромбоэдрическая, многоступенчатая, с периодом α = 4,123 A, углом α = 54° 10′. Плотность (при 20° C) 5,72 г/см3 ; коэффициент линейного теплового расширения 3,36 — 10 градусов ; электрическое сопротивление (температура 0° C) 35 — 10 — 6 Ом — см ; HB = 147 ; коэффициент сжимаемости (при температуре 30° C) 4,5×1 0-6 см 2 /кг. Температура плавления мышьяка альфа составляет 816°C при давлении 36 атмосфер.
При атмосферном давлении мышьяк сублимирует при температуре 615° C, не плавясь. Теплота сублимации составляет 102 кал/г. Пары мышьяка бесцветны, до температуры 800°C они состоят из As4молекул, от 800 до 1700 °C, состоящий из смеси As4и как2молекулы, выше 1700 °C только As2. Быстрая конденсация паров мышьяка на поверхности, охлаждаемой жидким воздухом, приводит к образованию желтых, прозрачных для мышьяка, мягких кристаллов кубической системы с плотностью 1,97 г/см 3. Известны и другие метастабильные модификации мышьяка: бета-марсеновая, аморфная, стеклообразная, с-марсеновая, желто-коричневая и дельта-марсеновая, коричневая, аморфная с плотностью 4,73, 4,97 и 5,10 г/см 3, соответственно. Выше температуры 270° С эти модификации превращаются в серый мышьяк.
СВОЙСТВА

Цвет при свежем разрушении — цинково-белый, оловянно-белый до светло-серого, быстро тускнеет из-за образования темно-серой черной смолы на корродированной поверхности. Твердость по Моосу 3 — 3,5. плотность 5,63 — 5,8 г/см3. Узнается по характерному чесночному запаху при ударе. Вырез идеален по длине и менее идеален по ширине. Излом зернистый. Удельный вес 5,63-5,78. Полоса серая, белая оловянная. Блеск металлический, интенсивный (на свежем изломе), быстро тускнеет и со временем становится тусклым на окисленной, почерневшей поверхности. Он является диамагнитным.

Мышьяк часто наблюдается в виде кальцинированных почкообразных поверхностей коры, в виде сталактитов и в виде раковинных образований с кристаллически-зернистой структурой в изломе. Природный мышьяк относительно легко распознать по форме преципитатов, почерневшей поверхности, высокому удельному весу, интенсивному металлическому блеску в свежем изломе и совершенной спайности. Под сварочной трубкой он испаряется, не плавясь (при температуре около 360°), выделяя характерный чесночный запах и белый как2О3на угле. Он переходит в жидкое состояние только под воздействием повышенного внешнего давления. В закрытой пробирке он образует зеркальное отражение мышьяка. При сильном ударе молотком он издает запах, напоминающий чеснок.
ПРОИСХОЖДЕНИЕ

Мышьяк встречается в гидротермальных месторождениях в виде постколлоидного образования в полостях, которые, вероятно, образовались в последние моменты гидротермальной активности. В сочетании с ним могут встречаться мышьяк, сурьма и, реже, сернистые соединения никеля, кобальта, серебра, свинца и других, а также неметаллические минералы.
В литературе встречаются ссылки на вторичное происхождение мышьяка в зонах выветривания месторождений мышьяковых руд, что в целом маловероятно, поскольку он очень нестабилен в этих условиях и полностью разлагается при быстром окислении. Черные корки состоят из тонкой смеси мышьяка и арсенулита (As2О3В конечном итоге образуется чистый арсенолит.
Концентрация мышьяка в земной коре низкая — 1,5 промилле. Он присутствует в почвах и минералах и может попасть в воздух, воду и почву в результате ветровой и водной эрозии. Кроме того, этот элемент попадает в атмосферу и из других источников. Вулканические извержения ежегодно выбрасывают в воздух около 3 000 тонн мышьяка, микроорганизмы производят 20 000 тонн летучего метиларсина в год, а сжигание ископаемого топлива выделяет 80 000 тонн за тот же период.
В СССР самородный мышьяк был обнаружен в различных месторождениях. Здесь следует упомянуть Садонское гидротермальное свинцово-цинковое месторождение, где он неоднократно наблюдался в виде почковидной массы на кристаллическом кальците с галенитом и сфалеритом. На левом берегу реки Хикой (Забайкалье) были обнаружены крупные скопления самородного мышьяка почковидной формы с концентрической структурой оболочки. При его добыче в стенках тонких жил, прорезающих старые кристаллические сланцы, наблюдался только кальцит в виде оторочки. Арсенит в виде фрагментов (рис. 76) был также найден в районе железнодорожной станции Джалинда, на сети Амурской железной дороги и в других местах.
В некоторых месторождениях Саксонии (Фрайберг, Шнееберг, Аннаберг и др.) самородный мышьяк был обнаружен в сочетании с соединениями мышьяка с кобальтом, никелем, серебром, самородным висмутом и др. Все эти и другие открытия этого минерала не имеют практического значения.
Этимология
Название мышьяк в русском языке происходит от слова «мышь», так как его соединения использовались для уничтожения мышей и крыс. Греческое название мышьяка происходит от персидского زرنيخ (zarnik), «желтая серьга». Популярная этимология восходит к греческому arsenikos — мышьяк.
Латинское название arsenicum является прямым заимствованием греческого arsenin. В 1789 году мышьяк был зарегистрирован как химический элемент А. Лавуазье под названием arsenic.
Нахождение в природе
Мышьяк является дисперсным элементом. Его содержание в земной коре составляет 1,7⋅1 0-4 массовых процента. В морской воде он составляет 0,003 мг/л. Этот элемент иногда встречается в природе в виде самородков — минералов, которые выглядят как блестящие металлически-серые раковины или плотные массы, состоящие из мелких зерен.
Известно около 200 минералов, содержащих мышьяк. В небольших концентрациях он часто встречается в ассоциации со свинцовыми, медными и серебряными рудами. Два природных минерала мышьяка в виде сульфидов (бинарных соединений с серой) встречаются довольно часто: оранжево-красный прозрачный реальгар AsS и лимонно-желтая сережка As.2S3. Минералом, имеющим промышленное значение для производства мышьяка, является арсенопирит (мышьяковая металлургия) FeAsS или FeS2-FeAs2(46 % As), арсенопирит (FeAs2) (72,8 % As), вскоре FeAsO4(Большая часть мышьяка извлекается как побочный продукт при переработке золотых, свинцово-цинковых, медно-медных и других мышьякосодержащих руд.


Месторождения
Наиболее важным промышленным минералом мышьяка является арсенопирит FeAsS. Существуют крупные медно-арсеновые месторождения в Грузии, Средней Азии и Казахстане, в США, Швеции, Норвегии и Японии, мышьяково-кобальтовые месторождения в Канаде и мышьяково-оловянные месторождения в Боливии и Англии. Также мышьяково-золотые месторождения есть в США и Франции. В России имеются многочисленные месторождения мышьяка в Якутии, на Урале, в Сибири, Забайкалье и на Чукотке.
Изотопы
Известно 33 изотопа и не менее 10 возбужденных состояний ядерных изомеров. Из этих изотопов только 75 As является стабильным, и природный мышьяк состоит только из этого изотопа. Самый долгоживущий радиоактивный изотоп, 73 As, имеет период полураспада 80,3 дня.
Открытие метода получения металлического мышьяка (серого мышьяка) приписывается средневековому алхимику Альберту Великому, родившемуся в XIII в. Однако гораздо раньше греческие и арабские алхимики умели получать мышьяк в свободной форме путем нагревания «белого мышьяка» (триоксида мышьяка) с различными органическими веществами.
Существует множество методов получения мышьяка: возгонка природного мышьяка, термическое разложение мышьяковистых силикатов, восстановление мышьяковистого ангидрида и т.д.
Для извлечения металлического мышьяка арсенопирит в настоящее время в основном нагревают в муфельных печах без подачи воздуха. При этом образуется мышьяк, пары которого конденсируются и превращаются в твердый мышьяк в железных трубах, выходящих из печей, и в специальных керамических контейнерах. Затем остаток в печах нагревается с притоком воздуха, и мышьяк преобразуется в качестве2O3. Металлический мышьяк извлекается в довольно небольших количествах, а большинство мышьякосодержащих руд превращаются в белый мышьяк, т.е. триоксид мышьяка — мышьяковый ангидрид As.2O3.
Основным методом добычи является обжиг сульфидных руд и последующее восстановление оксидов с помощью углерода:
Мышьяк в природе
В природной среде мышьяк встречается в основном в виде сульфидов. Известно около 120 минералов, содержащих мышьяк.
Наиболее распространенными являются арсенический пирит (также называемый арсенопиритом) FeAsS (46,0% As), арсенический пирит (леллинит) FeAs2(72,8% As), реальгар As4S4(70,1% As) и отолитовый As2S3(61,0% As). Были выявлены различные аллотропные модификации мышьяка.
Природный мышьяк на 100% состоит из стабильного изотопа 75As, который встречается в литосфере в количестве около 0,0005% по весу. Мышьяк распространен в виде сульфидов: аурический пигмент (золотой цвет), такой как2S2и мышьяк-пирит-колчедан FeAsS, который иногда встречается в свободном виде.
Физические свойства
При нормальных условиях металлический или серый мышьяк (альфа-арсенид) стабилен. Кристаллическая решетка серого мышьяка ромбоэдрическая, слоистая, с периодом α = 4,123 Å, углом α = 54° 10′.
Плотность (температура 20 °C) 5,72 г/см3; температурный коэффициент линейного расширения 3,36 — 10° c; удельное электрическое сопротивление (температура 0 °C) 35 — 10 — 6 Ом — см; HB = w 147; коэффициент сжимаемости (температура 30 °C) 4,5×10 — 6 см2/кг.
Мышьяк диамагнитен. Температура плавления мышьяка альфа составляет 816°C при 36 ат.
При атмосферном давлении мышьяк возгоняется при температуре 615°C, не плавясь. Теплота сублимации составляет 102 кал/г. Пары мышьяка бесцветны, до 800°C они состоят из молекул As4, от 800 до 1700°C они представляют собой смесь As4и как2и выше 1700°C только As.2.
При быстрой конденсации паров мышьяка на поверхности, охлаждаемой жидким воздухом, образуется желтый мышьяк — прозрачные мягкие кристаллы кубической системы с плотностью 1,97 г/см3.
Модификации
Известны и другие метастабильные модификации М.: b-арсеновая — аморфная стеклообразная, c-арсеновая — желто-коричневая и дельта-арсеновая — коричневая аморфная с плотностями 4,73, 4,97 и 5,10 г/см3 соответственно.
При температуре выше 270° C эти модификации переходят в серый мышьяк.
Химические свойства
При нагревании на воздухе мышьяк легко окисляется до As2O3. Измельченный мышьяк быстро сгорает ярким голубым пламенем и выделяет белый дым.2O3.
Азотная кислота и акварегия окисляют его до мышьяковой кислоты H3AsO4который при нагревании выделяет As2O6. Мышьяк соединяется непосредственно с галогенами, образуя галогениды: при нормальных условиях AsF является5— газ; AsF3, AsCl.3и AsBr3 — бесцветные, летучие жидкости.2I4и как2I3— красные кристаллы.
При нагревании с серой образуются сульфиды As4S4 (оранжево-красный) и As2S3(лимонно-желтый). Когда H2S в холодном растворе мышьяковой кислоты (или ее солей), бледно-желтый As.2S5.
В сплаве со многими металлами мышьяк образует арсениды. В большинстве случаев он легко растворим в твердых металлах.
Мышьяк образует непрерывные твердые растворы только с сурьмой. В сплавах железа, содержащих мышьяк, качество металла ухудшается с увеличением содержания углерода.
При взаимодействии М. или его соединений с водородом во время экстракции образуется очень токсичный газ — арсин или арсин AsH3. Он также образуется при разложении арсенидов разбавленными кислотами.
Исходным материалом для экстракции мышьяка и его соединений является триоксид As.2O3триоксид, который образуется при окислительном обжиге мышьяксодержащих руд и полиметаллических сульфидных руд с М-соединениями в качестве примесей.








