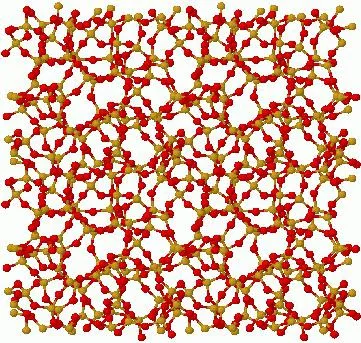
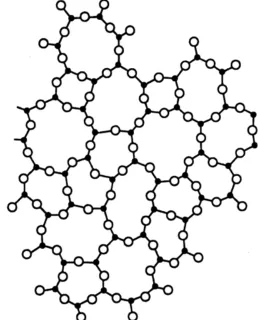
Водородные связи между молекулами воды обозначены черными линиями. Желтые линии указывают на ковалентные связи, удерживающие кислород (красный) и водород (серый).
Свойства вещества в разных агрегатных состояниях
Кумулятивные состояния материи — это состояния одного и того же вещества, а переходы между ними характеризуются скачкообразными изменениями в характере теплового движения, плотности, давления и других природных параметров.
Природа теплового движения молекул обусловлена характером их взаимодействий. Силы взаимодействия являются электромагнитными, быстрыми и сильно зависят от расстояния.
Если расстояние между молекулами в несколько раз превышает их размер, то взаимодействия очень малы и ими можно пренебречь. По мере уменьшения расстояния притяжение между молекулами увеличивается из-за перекрывания электронных путей и появления «общих» электронов у разных молекулярных индивидов (возникновение ковалентных связей). Однако при дальнейшем сближении между однородно заряженными отдельными ядрами начинают преобладать силы отталкивания.
Согласно природе теплового движения, существуют три основные ситуации для сцепления материи: твердое тело, жидкость и газ. Четвертая кумулятивная ситуация, которая возникает в основном при сгорании на Земле, — это живые существа.
При переходе из одного агрегатного состояния в другое различные части вещества могут находиться в разных ситуациях. Например, при таянии кусок льда плавает на воде. А когда она закипает, пузырек пара поднимается вверх по жидкости.
Одна фаза — это сочетание всех частей системы, которые имеют одинаковый состав и находятся в одном общем состоянии.
При таянии лед и вода образуют двухфазную систему.
Система «лед-вода-влажный воздух» — это трехфазная система.
Все фазы системы находятся в равновесии, что называется термодинамикой.
Понятие ближнего и дальнего классов используется для описания степени класса частиц материи.
Практически это класс взаимоперестановок индивидов и молекул вещества, происходящих только на диатомарных расстояниях, и наличие дизайна в соседних индивидах и молекулах.
Меньшими диапазонами являются твердые вещества (кристаллические и аморфные) и жидкости.
Большой диапазон — это порядок взаиморасположения индивидов и молекул материала, который повторяется на бесконечно больших расстояниях.
Ассортимент кристаллических твердых веществ велик.
п.2. Свойства твердых тел
В твердых телах частицы (молекулы, индивиды и ионы) расположены настолько близко друг к другу, что силы притяжения уравновешиваются силами отталкивания. Частицы колеблются вокруг определенной точки и не могут быть удалены от нее. Таким образом, твердое тело сохраняет как свою форму, так и объем.
Существует различие между кристаллическими и аморфными твердыми телами.
В кристаллических твердых телах частицы образуют «решетку» и имеют ближний и дальний классы. Твердые аморфы имеют лишь небольшую протяженность — их структура аналогична структуре жидкостей.
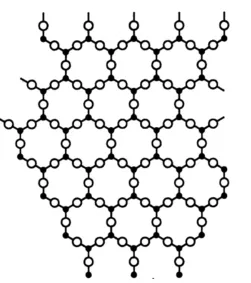 Атомная структура кристаллического твердого тела Атомная структура кристаллического твердого тела |
 Атомная структура аморфного твердого тела Атомная структура аморфного твердого тела |
Различие в структурных классах приводит к следующим свойствам кристаллических и аморфных твердых тел
Свойства твердых тел в зависимости от расположения частиц
Зависимость природных свойств от направления — Анизотропия
Зависимость физических свойств от направления — Изотропный
Восстановление формы и опухоли после прекращения внешнего воздействия — Гибкость
Изменение формы и опухоли после прекращения внешнего воздействия (без разрушения) — Пластичность
Фиксированная температура плавления
Инклюзивная температура плавления
п.3. Свойства жидкостей
Частицы (атомы или молекулы) вещества в жидком состоянии не имеют определенного положения, но они также не могут свободно перемещаться по всему объему. Они колеблются вокруг положения равновесия и часто перескакивают из одного положения равновесия в другое.
Поскольку частицы не удаляются друг от друга, жидкость сохраняет свой объем, но не форму. Они образуют поверхность в форме контейнера.
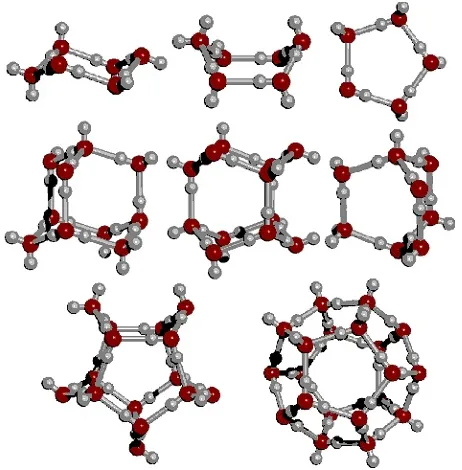
В жидкостях сохраняется почти такой же порядок. Притягательные силы между частицами достаточно сильны, чтобы приблизить их друг к другу. Силы притяжения позволяют молекулам жидкости образовывать кластеры.
Внимание. Если преподаватель обнаружит плагиат в вашей работе, у вас могут быть большие неприятности (вплоть до исключения из школы). Если вы не можете написать работу самостоятельно, вы можете заказать ее здесь.
Содержание
Схема атомной структуры аморфных (слева) и обычных (справа) кристаллических твердых тел.
Различают кристаллические и аморфные твердые тела (см. дальний и ближний порядок). Кристаллы характеризуются пространственной периодичностью в расположении равновесных позиций атомов. В аморфных твердых телах атомы колеблются вокруг неупорядоченного расположения точек1. Согласно классическим представлениям, устойчивое состояние твердого тела (минимум динамической энергии) — это кристаллическое состояние. Аморфные твердые вещества находятся в переходном состоянии и со временем должны перейти в кристаллическое состояние, но время кристаллизации настолько велико, что переход вообще не происходит.
-
и молекулы, составляющие твёрдое тело, плотно упакованы вместе. Другими словами, молекулы твёрдого тела практически сохраняют своё взаимное положение относительно других молекул 2 и удерживаются между собой межмолекулярным взаимодействием.
- Многие твёрдые тела содержат в себе кристаллические структуры. В минералогии и кристаллографии под кристаллической структурой подразумевается определённый порядок атомов в кристалле. Кристаллическая структура состоит из элементарных ячеек, набора атомов расположенных в особенном порядке, который периодически повторяется во всех направлениях пространственной решётки. Расстояния между элементами этой решётки в различных направлениях называют параметром этой решётки. Кристаллическая структура и симметричность играют роль в определении множества свойств, таких как спайность кристалла, электронная зонная структура и оптические свойства.
- При применении достаточной силы любое из этих свойств может быть нарушено, вызывая остаточную деформацию.
Часть физики, изучающая твердые тела, называется физикой твердого тела (подраздел естественной конденсированной материи), и ее развитие обусловлено потребностями технологии. Физика твердого тела делится на несколько областей, разделенных по признаку определения либо объекта исследования (например, металлофизика, полупроводники, магнетизм), либо метода исследования (например, рентгеноструктурный анализ). спектроскопия и т.д.) или специфические свойства (механические, тепловые и т.д.)1.
Материаловедение занимается в основном изучением свойств твердых тел, таких как твердость, прочность на разрыв, устойчивость к нагрузкам и фазовые превращения. Это в значительной степени соответствует предмету, изучаемому в физике твердого тела. Химия твердого тела пересекается с проблемами, решаемыми в обеих дисциплинах, но в первую очередь это синтез новых материалов.
Изучение свойств твердых тел интегрировано в более широкую область физического твердого тела, развитие которой обусловлено потребностями технологии. Физика твердого тела может быть разделена на различные дисциплины, отличающиеся либо предметом изучения (например, металлофизика, полупроводники, магнетизм), либо методом исследования (например, рентгеноструктурный анализ, лучевая спектроскопия). и т.д.) или по специфическим свойствам (механическим, тепловым и т.д.).
Самым легким из известных твердых материалов является аэрогель. Некоторые виды аэрогелей имеют плотность 1,9 мг/см³ или 1,9 кг/мл (1/530 от плотности воды).
Классификация твёрдых тел
Различают ионную, ковалентную, металлическую и другие виды связи между атомами. Электрические и некоторые другие свойства твердых тел определяются в основном характером движения внешних электронов их атомов1.
- проводники — зона проводимости и валентная зона перекрываются, таким образом электрон может свободно перемещаться между ними, получив любую допустимо малую энергию. Таким образом, при приложении к твердому телу разности потенциалов, электроны смогут свободно двигаться из точки с меньшим потенциалом в точку с большим, образуя электрический ток. К проводникам относят все металлы.
- полупроводники — зоны не перекрываются и расстояние между ними составляет менее 4эВ. Для того, чтобы перевести электрон из валентной зоны в зону проводимости требуется энергия меньшая, чем для диэлектрика, поэтому чистые (собственные, нелегированные) полупроводники слабо пропускают ток.
- диэлектрики — зоны не перекрываются и расстояние между ними составляет более 4эВ. Таким образом, для того, чтобы перевести электрон из валентной зоны в зону проводимости требуется значительная энергия, поэтому диэлектрики ток практически не проводят.
По своим магнитным свойствам твердые тела можно разделить на объекты с антимагнитной, парамагнитной и регулярной магнитной структурой1.
Историческая справка
Твердые материалы (минералы и минералогия) изучаются уже давно, но комплексное изучение и систематизация информации об их свойствах начались в 17 веке. С тех пор было открыто множество эмпирических законов, объясняющих действие механических сил, изменений температуры, света, электромагнитных полей и т.д. В твердых телах. Формула:.
Уже в первой половине 19 века были сформулированы основные принципы теории упругости. Это была концепция твердого тела, характеризующегося как непрерывная среда.
Первая идея такого рода была сформулирована Огюстом Браве в 1848 году в книге «Николас Стено» (Nicholas Steno Treat). Общее представление о кристаллической структуре твердых тел как о множестве людей, для которых характерно гладкое расположение, было создано Огюстом Браве в 1848 году. (переведен на английский язык в 1848 году). Николас Стено (1669), Рене Юст Хоуи (1784), Исаак Ньютон в «Математических началах физической философии» (1686)., Огюстен-Луи Коши (1830) и другие.
Использование твердых веществ является очень перспективным. С развитием науки список их полезных свойств постоянно расширяется. Следовательно, будущее, как и настоящее, может только выиграть от их использования.
Типы кристаллических твердых веществ
В твердом состоянии почти все вещества имеют кристаллическую структуру. Структуры различаются. Кристаллическая решетка содержит различные частицы и химические вещества в узлах. Они согласились получить собственное имя. Каждый вид имеет свои характерные свойства.
- В кристаллической решетке металла узлы содержат только положительно заряженные ионы химических веществ. Между ними находятся свободные электроны, через которые идеально проходит тепловая и электрическая энергия. Именно поэтому все металлы отличаются такой характеристикой, как проводимость.
- В молекулярной кристаллической решетке связь между частицами характеризуется слабостью. Вещества этого типа отличаются легкостью кипения и плавления. Они отличаются своей летучестью, из-за чего имеют определенный запах. К таким твердым веществам относятся лед, сахар. Молекулярные движения в твердых телах этого типа отличаются своей активностью.
- В атомной кристаллической решетке частицы твердого тела связаны ковалентной связью. Он отличается своей прочностью. Благодаря этому такие вещества имеют высокую температуру плавления и кипения. К этому типу относятся кварц и алмаз.
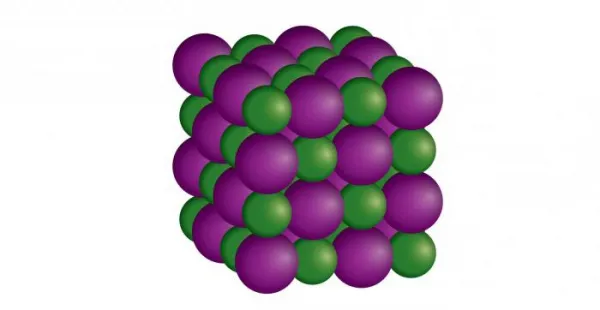
- В ионной кристаллической решетке соответствующие частицы, положительно и отрицательно заряженные, чередуются в узлах. Они удерживаются вместе за счет электростатического притяжения. Такой тип решетки существует в щелочах, солях, основных оксидах. Многие вещества этого типа легко растворяются в воде. Благодаря достаточно прочной связи между ионами они тугоплавкие. Практически все они не имеют запаха, так как нелетучие. Вещества с ионной решеткой не способны проводить электрический ток, так как в их составе нет свободных электронов. Типичным примером ионного твердого вещества является поваренная соль. Эта кристаллическая решетка делает его хрупким. Это связано с тем, что любое его смещение может привести к появлению сил отталкивания ионов.

Общие понятия о твердом теле
Твердые тела и вещества — это, по сути, одно и то же. Эти термины относятся к одной из четырех ситуаций. Твердые тела имеют фиксированную форму и характерное тепловое движение людей. Кроме того, последние имеют небольшие колебания вблизи положения равновесия. Отрасль науки, изучающая состав и внутреннюю структуру, называется физическим твердым телом. Существуют и другие важные области знаний, связанные с этими веществами. Внешние воздействия и изменения формы в результате движения называются динамикой деформируемых тел.
Благодаря различным свойствам твердых тел, они нашли применение в различных технологических устройствах, созданных руками человека. В большинстве случаев их использование основывалось на таких свойствах, как твердость, объем, масса, эластичность, пластичность и хрупкость. Современная наука позволяет использовать и другие свойства твердых тел, которые могут быть обнаружены только в лабораторных условиях.
Что такое кристаллы
Кристаллы — это твердые тела, в которых частицы расположены в определенном порядке. Каждое химическое вещество имеет свою уникальную структуру. Индивиды образуют трехмерную периодическую схему, называемую кристаллической решеткой. Твердые тела имеют различные структурные симметрии. Кристаллическое состояние твердого тела считается постоянным, поскольку оно обладает минимальным количеством потенциальной энергии.
Подавляющее большинство (природных) твердых тел состоит из огромного количества случайно ориентированных отдельных гранул (кристаллов). Такие вещества называются поликристаллическими. К ним относятся технические сплавы и металлы, а также многие горные породы. Природные или синтетические монокристаллы называются монокристаллами.
В большинстве случаев эти твердые вещества образуются в состоянии жидкой фазы, представляющей собой расплав или раствор. Иногда они образуются в газообразном состоянии. Этот процесс известен как кристаллизация. Благодаря достижениям науки и техники процесс выращивания (синтеза) различных веществ происходит в промышленных масштабах. Большинство кристаллов имеют естественную многогранную форму. Их размеры варьируются в широких пределах. Например, природный кварц (каменные кристаллы) весит до нескольких сотен килограммов, в то время как алмазы весят до нескольких граммов.
В аморфных твердых телах атомы постоянно совершают колебания вокруг беспорядочно расположенных точек. Они поддерживают некоторый ближний порядок, но не дальний. Это связано с тем, что их молекулы находятся на таком расстоянии друг от друга, что их размеры можно сравнить. Наиболее распространенным примером таких твердых тел в нашей жизни является стеклообразное состояние. Аморфные вещества часто рассматриваются как жидкости с бесконечно высокой вязкостью. Время их кристаллизации иногда очень велико, а иногда они могут вообще не появляться.
Именно вышеупомянутые свойства этих веществ делают их уникальными. Аморфные твердые вещества считаются нестабильными, поскольку со временем они могут кристаллизоваться.
Молекулы и атомы, из которых состоят твердые тела, имеют плотную структуру. Они фактически удерживают свое положение относительно других частиц и прилипают друг к другу благодаря межмолекулярным взаимодействиям. Расстояния между молекулами твердого тела в различных направлениях называются параметрами решетки. Структура материала и его симметрия определяют многие его свойства, такие как электронные полосы, разделение и оптика. Если к твердому телу приложить достаточно большую силу, эти свойства могут быть нарушены определенным образом. В этом случае твердое тело постоянно деформируется.
Атомы твердого тела испытывают колебательные движения, которые определяют их тепловую энергию. Они незначительны и поэтому могут наблюдаться только в лаборатории. Молекулярная структура твердого тела влияет на его свойства различными способами.