Резюме. Материя состоит из молекул, молекулы состоят из людей, а люди с одинаковым ядерным зарядом принадлежат к одному химическому элементу.
Физика (7 класс)/Начальные сведения о веществе
Уже 2 500 лет назад некоторые ученые строили догадки о структуре материи. Греческий ученый Демократ (460-370 гг. до н.э.) считал, что вся материя состоит из мелких частиц. Эта идея превратилась в научную теорию только в 18 веке и получила дальнейшее развитие в 19 веке. Появление концепции строения материи позволило не только объяснить многие явления, но и предсказать, как они могут развиваться при определенных обстоятельствах.
Многие эксперименты подтверждают признание структуры материи. Давайте рассмотрим некоторые из них.
Попробуйте затянуть теннисный мяч. Это уменьшает количество воздуха, заполняющего шар. Объем шара или кусочков воска в шаре также может быть уменьшен путем приложения некоторой силы.
Объем тела также изменяется при нагревании или охлаждении.
Эксперимент. Возьмите медный или латунный шарик, который проходит через кольцо, когда оно не нагрето. Если шар нагрет, то при расширении он не пройдет через кольцо. Через некоторое время, после охлаждения пули (и, следовательно, уменьшения ее размеров), она частично нагревает (и, следовательно, расширяет) кольцо и снова проходит через него.
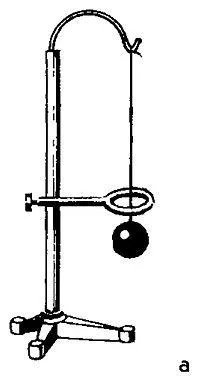
Это изображение показывает, что в ненагретом состоянии бронзовая сфера легко проходит через кольцо.
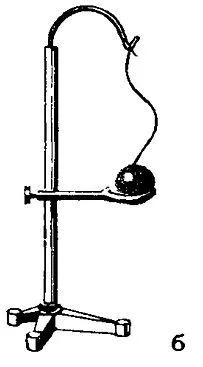
Здесь видно, что в нагретом состоянии вместо того, чтобы расширяться и проходить через кольцо, оно задерживается.
С помощью эксперимента определите, как изменяется объем жидкости при нагревании.
Закройте бутылку, наполненную водой, и закупорьте ее пробкой. Пропустите стеклянную трубку через пробку. Вода частично заполняет трубку. Обратите внимание на уровень жидкости в трубке. Нагрейте бутылку, и вы заметите, что через некоторое время уровень воды повысится.
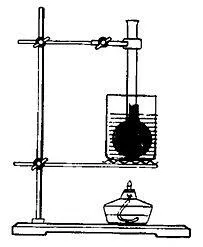
Вода не нагревается и только заполняет трубку. Уровень воды в трубе низкий.
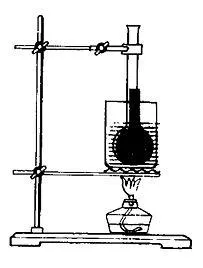
Вода нагревается, начинает расширяться и заполнять свободное пространство. Уровень воды в трубе повысился.
Поэтому нагревание увеличивает объем, а охлаждение уменьшает его.
Давайте попробуем объяснить, почему изменяется объем.
Очевидно, что все вещества состоят из отдельных частиц с пространством между ними. Когда частицы удаляются друг от друга, объем увеличивается. А когда частицы движутся ближе друг к другу, объем уменьшается.
Следующий вопрос. Если тело состоит из мелких частиц, почему оно твердое?
Современная наука доказывает, что частицы материи настолько малы, что мы не можем их увидеть.
Чтобы подтвердить, что частицы материи малы, давайте проведем эксперимент.
Растворите мелкие частицы гуаши в емкости с водой. Через некоторое время вода в нем становится синей. Вылейте воду в другую емкость и наполните ее чистой водой. Раствор во второй емкости будет слабее, чем в первой. Затем повторите весь процесс, но используйте воду из второй емкости. В третьей емкости вода еще слабее, чем во второй емкости, и намного слабее, чем в первой емкости.
Молекулы. править
Все вещества состоят из отдельных частиц — это доказано современной наукой. Эти частицы получили название мориа (в переводе с латинского — «маленькая масса»).

Молекулы вещества — это мельчайшие частицы определенного вещества.
Например, самой маленькой частицей воды является молекула воды. Более мелкие частицы соли — это молекулы соли.
Представьте себе, каков размер молекулы.
Если 10 000 000 (или 10-7 градусов Цельсия) молекул воды могут быть уложены в непосредственной близости друг от друга, потребуется только одна нить диаметром 2 мм. Благодаря небольшому размеру молекул можно создавать тонкие пленки различных веществ. Например, капля масла может быть распределена на воде слоем толщиной 0,000002 м (или 2 при силе 10-6).
Даже маленькие тела состоят из огромных молекулярных масс. Например, крупинка соли или сахара содержит очень большое количество молекул. Считается, что в 1 см³ воздуха содержится примерно от 27 до 1018 молекул. Чтобы понять, насколько велико это число, представьте, что Через маленькое отверстие в воздухе каждую секунду проходит 1 миллион молекул. Вышеупомянутое количество молекул пройдет через отверстие в течение следующих 840 000 лет.
Из-за своего очень маленького размера молекулы невидимы невооруженным глазом или в обычные микроскопы. Однако с помощью специального прибора, электронного микроскопа, самые крупные из них можно было сфотографировать. На рисунке показано расположение молекул белка.
Окружающие нас тела могут выглядеть одинаково, но быть разными. В природе вы не найдете двух снежинок, песчинок, людей или животных. Они выглядят совершенно одинаково по отношению друг к другу.
Ученые с помощью экспериментов доказали, что молекулы разных веществ отличаются друг от друга, а молекулы одного и того же вещества одинаковы. Например, вода из сока или молока неотличима от воды, полученной путем дистилляции морской воды. Молекулы воды одинаковы. Ни одно другое вещество не может состоять из таких молекул.
Молекулы, с другой стороны, состоят из еще более мелких частиц, или атомов.
Например, самая маленькая частица воды — это молекула воды. Он состоит из трех атомов: двух атомов водорода и одного атома кислорода. Из урока химии мы знаем, что вода называется H2O. H — атом водорода, а O — атом кислорода.
Молекулы обычно изображаются схематично. Другими словами, используется молекулярная модель. На рисунке изображены две молекулы воды. Когда две молекулы воды разделяются, образуются два атома кислорода и четыре атома водорода. На следующем рисунке показано, что каждые два атома водорода могут соединиться и образовать молекулу водорода, а атомы кислорода могут соединиться и образовать молекулу кислорода.

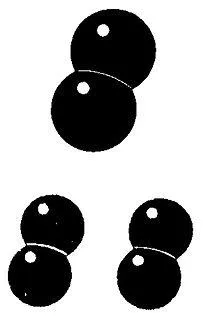
Атомы также состоят из маленьких частиц, о которых вы узнаете на уроках химии в 8 классе.
Диффузия в газах, жидкостях и твердых телах. править

Известно, что если поместить в комнату плохое вещество, например, духи или нафталин, то вскоре запах будет ощущаться по всей комнате. Распространение запаха происходит благодаря тому, что молекулы ароматизатора (или нафталина) находятся в движении.
Поэтому возникает вопрос, почему запах в помещении распространяется не сразу, а через некоторое время.
Причина в том, что движению молекул аромата в определенных направлениях препятствует движение молекул воздуха. Молекулы аромата (или нафталина) в процессе сталкиваются с молекулами газа, входящего в состав воздуха. Они постоянно меняют направление и при случайном движении влетают в комнату.
Давайте попробуем провести эксперимент, который можно объяснить только тем, что объект состоит из молекул, которые постоянно движутся.
Налейте немного темно-синего сульфата меди в мензурку (или мензурки). Осторожно добавьте сверху чистую воду.

Сначала между водой и сульфатом меди существует сильная граница, но через несколько дней она становится не такой сильной. Граница, отделяющая одну жидкость от другой, исчезает через две-три недели. В емкости образуется однородная жидкость светло-голубого цвета. Это означает, что жидкости смешиваются.
Наблюдаемое явление объясняется тем, что молекулы воды и сульфата меди обмениваются позициями вблизи границы раздела между этими жидкостями. Интерфейс размыт. В итоге молекулы сульфата меди переместились в нижний слой воды, а молекулы воды — в верхний слой сульфата меди.
Если оставить стекло на две-три недели, границы стекла еще больше размываются и постепенно полностью исчезают. Вся вода становится синей. Это происходит из-за того, что молекулы постоянно беспорядочно перемещаются и распространяются по опухоли. Жидкость в емкости становится однородной.
Явление взаимопроникновения молекул одного вещества между молекулами другого вещества называется диффузией.
Диффузия также происходит в твердых телах, но с еще более медленной скоростью.
Например, очень гладко отполированные пластины из свинца и золота укладываются друг на друга и на них помещаются грузы. При комнатной температуре (20°C) через 4-5 лет золото и свинец проникают друг в друга на расстояние около 1 мм. Во всех вышеперечисленных экспериментах наблюдается взаимопроникновение, или диффузия, молекул вещества.
Диффузия играет важную роль в природе. Так, например, диффузия поддерживает однородный состав атмосферы вблизи поверхности Земли. Диффузия растворов различных солей в почве способствует нормальному питанию растений и других организмов.
На становление атомной и молекулярной оптики повлияли работы многих ученых. Учение об атомных молекулах впервые было разработано и использовано в химии великим русским ученым М. В. Ломоносовым. Основные принципы учения были сформулированы в его работе «Элементы математической химии» (1741) и ряде других работ.
Что внутри атома

Миф о неделимом атоме стал очевидным, когда британский физик Джозеф Джон Томпсон в 1897 году открыл отрицательно заряженную элементарную частицу — электрон. Он также создал первую электронную модель атома, известную как «модель сливового пудинга». В этой модели атомы представлены в виде сфер, заполненных положительно заряженной материей, в которой электроны размещены в хлебе, как кишмиш.
Неточность этой модели была доказана британским физиком сэром Эрнестом Резерфордом. Он экспериментально установил, что положительно заряженная часть человека сосредоточена в очень малых количествах. Эта часть называется ядром человека. Более 99,9% общей массы атома сосредоточено в ядре. И хотя электроны не встроены в ядро, они вращаются вокруг ядра по круговым орбитам, подобно тому, как планеты вращаются вокруг солнца в Солнечной системе. Модель Резерфорда для отдельных людей была названа планетарной моделью.
В конце концов, ядра тоже делятся. Она состоит из положительно заряженных элементарных частиц, называемых протонами, и незаряженных частиц, называемых нейтронами. Протоны и нейтроны связаны друг с другом ядерными силами, которые раздвигают их друг от друга.
Протон был открыт Резерфордом в 1919 году, а нейтрон — студентом Резерфорда Джеймсом Чедвиком в 1932 году. Протоны и нейтроны имеют одинаковую массовую величину. Заряд протона такой же, как и заряд электрона.
Протоны и нейтроны называются нуклонами. Эти частицы считались рудиментарными до середины 20-го века. Однако было обнаружено, что они тоже имеют сложный состав и состоят из других частиц.
Понятие об элементарных частицах
Что такое субатомная частица? Физики рассматривают его как маленький объект, который невозможно проанализировать по составляющим его элементам. Науке уже известно более 350 частиц, которые можно назвать элементарными. Их изучает физика частиц.
Однако не все субатомные частицы имеют право называться элементарными частицами. Некоторые из них имеют сложную структуру, тем не менее, их невозможно разделить на составляющие. Поэтому их продолжают называть элементарными частицами. Другие субатомные частицы, которые не имеют сложной структуры, называются элементарными частицами.
Помимо массы и заряда, очень важным свойством элементарных частиц является спин — собственный импульс частицы. Это квантовая функция. Она не зависит от движения частицы в пространстве. Аналогов в классической инженерии не существует. Spin может принимать как полуцелые, так и целые числа. Ученым известны частицы со спином 0, 1 / 2, 1, 3 / 2 и 2.
В зависимости от значения спина все элементарные частицы делятся на две категории: бозоны и частицы Ферми. Бозон — частицы с целочисленным спином. Частицы Ферми — частицы с половиной целочисленного спина.
Стандартная модель
Все известные науке элементарные частицы и взаимодействия между ними (за исключением гравитации) объясняются физической теорией, называемой Стандартной моделью. В этой теории материя и силы взаимодействия разделены.
В Стандартной модели элементарные частицы с частицами Ферми с половинным спином считаются «кирпичиками материи», а частицы с бозонами с целым спином — носителями взаимодействия.
Частицы Ферми подразделяются на кварки и лептоны.
Интересный факт: если в пище не хватает химических элементов в виде ионов или молекул, мы не чувствуем сытости. Возникает подсознательное стремление восполнить существующий дефицит другими компонентами пищи, что часто приводит к нарушению обмена веществ и ожирению.
Вещества — скопления очень маленьких компонентов
Исследование частиц — это почти полицейская история. Великий русский ученый М. Ломоносов часто использовал термины «тело ‘атомы’ и ‘молекулы’. Все было очень запутанно: делима ли личность или нет, из чего она состоит?
Согласно решению Международного совета химиков от 1860 года, атом — это мельчайшая частица, из которой состоит простое или сложное вещество. Молекула — это система ядер и электронов двух или более атомов. Частицы невидимы невооруженным глазом и могут быть восприняты только под мощным увеличением электронного микроскопа.
Атомы, изотопы
Атом состоит из ядра и электронов. Первая заряжена положительно. В этой области отрицательно заряженные электроны движутся с большой скоростью. Ядро содержит элементарные частицы: протоны (положительные) и нейтроны (отрицательные).
Атомы одного и того же элемента имеют разные массы и свойства, если у них одинаковое число протонов и разное число нейтронов. Это изотопы. Водород с одним протоном в ядре является самым распространенным протоном во Вселенной. Дейтерий, в ядре которого один протон и один нейтрон, является самым тяжелым изотопом. Легенда о «живой» и «мертвой» воде, вероятно, возникла из-за токсичности тяжелой воды, содержащей дейтерий.
Различные неорганические вещества, минералы, горные породы и многочисленные органические соединения обусловлены
- идентичностью частиц одного вещества;
- наличием разных структурных единиц (атомов, молекул, ионов);
- отличиями зарядов, масс и размеров видов атомов (химических элементов);
- способностью атомов и молекул терять или приобретать электроны, превращаясь в ионы — заряженные частицы;
- огромным количеством электронных конфигураций, кристаллических структур;
- различиями в энергетическом состоянии частиц.
Интересный факт: атомы Na, K, Ca и Cl опасны для жизни при попадании в организм, в то время как ионы Na+, K+, Ca2+ и Cl- безопасны и необходимы для организма.
Особенности строения веществ
Вещества могут быть молекулярными или ионными. Газообразный водород, кислород, двуокись углерода, азот, хлор и аммиак — это маленькие молекулы с небольшой массой. Они имеют относительно низкие температуры плавления и кипения.
Соли — это преимущественно ионные вещества. Инертные газы, алмаз и графит состоят исключительно из атомов. Структура металлов характеризуется наличием атомов, ионов и «электронных газов». Широкий спектр химически чистых и высокоочищенных веществ используется в химии, фармацевтике и других продуктах.
Интересный факт: знания о веществах представляют практический интерес для широкой общественности. Можно сэкономить деньги при покупке лекарств. Цена оригинального препарата включает маркетинговые расходы (до 90% от стоимости препарата). Генерические лекарства дешевле оригинальных. Они содержат одни и те же активные ингредиенты, а различия заключаются в производстве, составе и количестве клинических испытаний.