Метод заключается в измерении диаметра капли жидкости, вращающейся в более тяжелой жидкости. Этот метод измерения подходит для измерения низких или чрезвычайно низких значений межфазного давления. натяжения. Он часто используется для микроэмульсий, чтобы измерить эффективность поверхностно-активных веществ при добыче нефти, а также для определения адсорбционных свойств.
Свойства жидкостей. Поверхностное натяжение
Вещество в жидком состоянии характеризуется чрезвычайно плотным расположением молекул друг относительно друга. В отличие от кристаллических твердых тел, молекулы которых образуют упорядоченные структуры по всему объему кристалла и ограничены в своих тепловых колебаниях фиксированными центрами, молекулы жидкости обладают значительной степенью свободы. Каждая отдельная молекула жидкости, как и в твердых телах, «сдавливается» соседними молекулами и может совершать тепловые колебания вблизи положения равновесия. Однако в какой-то момент каждая молекула может переместиться на соседнее свободное место. Такие движения в жидкостях происходят довольно часто, поэтому молекулы не привязаны к определенным центрам, как в кристаллах, а могут перемещаться по всему объему жидкости. На этом факте основана текучесть жидкостей.
Благодаря сильным взаимодействиям между тесно связанными молекулами, они могут образовывать локальные, т.е. нестабильные, упорядоченные группы из многих молекул. Это явление называется квазипорядком (рис. 3.5.1).
Рисунок 3. 5. 1. Пример молекул ближнего порядка жидкости и молекул дальнего порядка кристаллического вещества: 1 — вода; 2 — лед.
Свойства жидкостей
На рисунке 3.5.2 на примере воды показано различие между газом и жидкостью. Молекула воды, H 2 O, состоит из одного атома кислорода и двух атомов водорода, расположенных под углом 104°. В среднем расстояние между молекулами пара в десять раз больше, чем расстояние между молекулами воды. На рисунке 3.5.2 показана структура молекулы воды в отличие от рисунка 3.5.1, на котором молекулы воды выглядят как сферы.
Рисунок 3.5.2: Водяной пар ( 1 ) и вода ( 2 ). Молекулы воды увеличиваются в 5 — 10 7 раз.
Сжимаемость жидкостей, т.е. изменение объема вещества при изменении давления, в десять или сто тысяч раз меньше, чем у газов, из-за плотности молекул. Например, чтобы изменить объем воды всего на 1 %, давление должно быть увеличено в 200 раз. Такое повышение давления по сравнению с атмосферным может быть достигнуто на глубине около 2 к м.
Подобно твердым телам, жидкости также склонны изменять свой объем при изменении температуры. Если разница температур не слишком велика, то относительное изменение объема Δ V V 0 пропорционально изменению температуры Δ T, что можно представить следующим образом:
Где коэффициент β представляет собой температурный коэффициент объемного расширения. В жидкостях этот коэффициент во много раз превышает значение такого же у твердых тел.
Например, в воде при температуре 20 °C β при ≈ 2 — 10 — 4 К — 1, в стали β при t ≈ 3, 6 — 10 — 5 К — 1, в кварцевом стекле β при ≈ 9 — 10 — 6 К — 1 .
Тепловое расширение воды имеет важное значение для жизни на Земле. При температуре ниже 4 °C вода начинает расширяться по мере уменьшения температуры β.< 0. Максимальную плотность ρ в = 10 3 к г / м 3 вода приобретает при температуре 4 ° С .
Когда вода замерзает, она расширяется, поэтому лед продолжает плавать на поверхности замерзшей воды. Температура замерзшей воды подо льдом равна 0 °C. На дне водоема, т.е. в более плотных слоях воды, температура остается на уровне около 4 °C.
Поверхностное натяжение
Свободная поверхность жидкостей — одно из самых интересных их свойств. В отличие от газов, жидкость не заполняет весь объем емкости, в которой она находится. Между жидкостью и газом, возможно, паром, существует граница раздела, которая подвергается особым условиям по сравнению с остальной частью жидкости. В отличие от молекул на дне жидкости, молекулы на границе раздела не окружены со всех сторон другими молекулами той же жидкости. В среднем силы межмолекулярных взаимодействий, оказываемых соседними молекулами на одну из молекул внутри жидкости, уравновешивают друг друга. Каждая отдельная молекула в пограничном слое притягивается молекулами внутри жидкости. В этом случае силы, действующие на на такую молекулы жидкости молекулами газа можно пренебречь. Это создает равновесную силу внутри жидкости. Поверхностные молекулы втягиваются внутрь жидкости под действием межмолекулярных притягательных сил. Однако все молекулы, включая молекулы в пограничном слое, должны находиться в состоянии равновесия. Это достигается за счет уменьшения расстояния между молекулами в пограничном слое и их ближайшими соседями в жидкости. Как показано на рисунке 3.1.2, силы отталкивания развиваются по мере уменьшения расстояния между молекулами. В случае, когда среднее значение расстояния между молекулами в жидкости равно r 0, молекулы являются поверхностного Молекулы слоя плотнее и поэтому имеют дополнительный запас потенциальной энергии по сравнению с внутренними молекулами, как показано на рисунке 3.1.2.
Стоит отметить, что чем плотнее поверхностного слой не вызывает заметного изменения объема жидкости из-за крайне низкой сжимаемости.
Силы межмолекулярного взаимодействия совершают положительную работу при движении молекулы от поверхности к внутренней части жидкости. Напротив, чтобы переместить некоторое количество молекул из глубины жидкости к поверхности, т.е. увеличить площадь поверхности жидкости, внешние силы должны совершить положительную работу, пропорциональную изменению Δ S в поверхности Δ A n e w :
Δ A in n e w = σ ∆ S ,
где коэффициент σ называется коэффициентом поверхностного натяжения ( σ > 0 ) .
Из вышесказанного следует, что коэффициент поверхностного натяжения — это величина, соответствующая работе, необходимой для увеличения площади поверхности жидкости на единицу при постоянной температуре.
В С И коэффициент поверхностного натяжения Она измеряется в джоулях на метр квадратный ( Дж / м 2 ) или в ньютонах на метр ( 1 Н / м = 1 Дж / м 2 ).
По сравнению с молекулами внутри жидкости, молекулы в поверхностного жидкого слоя обладают избыточной потенциальной энергией. Динамическая энергия E p поверхности жидкости пропорциональна ее площади и выражается следующей формулой:
E p = A in n e w = σ S .
Из механики известно, что равновесное состояние системы соответствует минимальному значению ее динамической энергии. Следовательно, свободная поверхность жидкости стремится уменьшить свою площадь. По этой причине свободная капля жидкости принимает сферическую форму.
Жидкость ведет себя таким как если бы существовали силы, действующие по касательной к поверхности, которые уменьшают эту поверхность. Эти силы называются силами поверхностного натяжения .
Я смешал все ингредиенты для раствора и использовал трубку для выдувания мыльных пузырей. Мыльные пузыри были маленькими, трудно выдувались и быстро лопались.
Что такое поверхностное натяжение и капиллярность
Молекулярное движение жидких частиц в основном представляет собой колебательное движение вокруг центрального положения. Поступательное движение ограничено обменом позициями с соседними частицами.
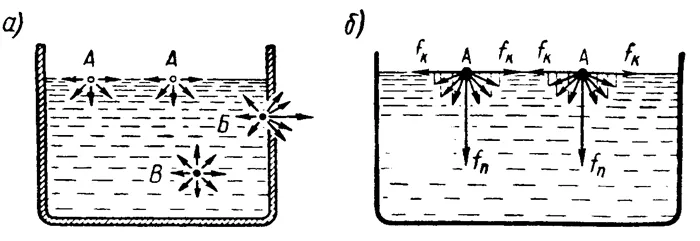
Рассмотрим молекулярные силы, действующие на молекулы B и A на фоне и в поверхностном Жидкий слой (рисунок 2, а). Молекула B со всех сторон окружена другими молекулами. Притягательные силы этих молекул действуют одинаково во всех направлениях на молекулу B, которая находится в равновесии.
Молекула A окружена молекулами жидкости только с нижней стороны, в то время как она окружена молекулами газа — воздуха или водяного пара — притягательная сила которых ничтожна.
Любая сила, действующая на молекулу A со стороны других молекул жидкости, может быть разделена на две составляющие, одна из которых направлена вдоль (тангенциально) поверхности, а другая — перпендикулярно ей.
Если сложить компоненты, перпендикулярные поверхности, то получится сила fпнаправлена в глубину жидкой массы, тангенциальные составляющие дают равные и противоположные силы fквдоль поверхности (Рисунок 2, б).
Что такое молекулярное давление жидкости
Силы fп оказывают на жидкость давление, которое сближает молекулы и уравновешивается их отталкивающими силами. Это давление называется молекулярным давлением жидкости.
Молекулярное давление не действует на тело, погруженное в жидкость (и поэтому не может быть определено приборами), так потому что она вызвана силами, действующими только между молекулами самой жидкости.
В зависимости от силы молекулярных сил они составляют порядка десятков тысяч атмосфер. Благодаря его наличию давление, вызванное внешними силами, которое значительно ниже, не вызывает дополнительного сжатия жидкости.
Это явление называется несжимаемостью жидкости.
Силы fкf силы, которые нейтрализуют каждую молекулу в отдельности, одновременно связывают их вместе дополнительной притягивающей силой, подобной той, которая возникает между молекулами в растянутой эластичной пленке. Совокупное действие этих сил называется поверхностным натяжением жидкости.
Поверхностное натяжение жидкости
Поверхностное натяжение Жидкости характеризуются силой F пкоторый наносится на контур, ограничивающий поверхность жидкости.
Эта сила действует в любой точке контура по касательной к поверхности жидкости и перпендикулярно линии контура. В полном объеме он действует так, что приводит к уменьшению свободной поверхности жидкости.
Эта сила для смачивания жидкостей уравновешивается силой равной величины и противоположного направления F’ п сцепление между молекулами жидкости и веществом стенок емкости, которое ограничивает свободную поверхность жидкости.
Наличие силы поверхностного натяжения можно продемонстрировать, например, в экспериментах с мыльными пленками.
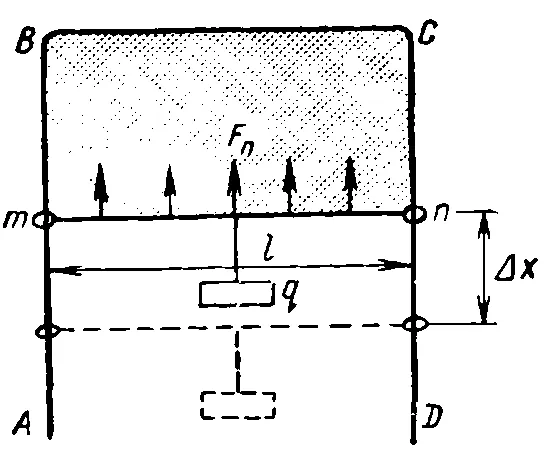
Мыльная пленка в воде образуется на проволочной раме ABCD (рис. 3) со слегка подвижной поперечной планкой tn.
Пленка тянет брусок вверх, а чтобы удержать его в нужном положении, он прикреплен к грузу q. Груз q — это гиря.
Это уравновешивает силу поверхностного натяжения с обеих сторон фольги), действующих на длину l перекладины.
Коэффициент поверхностного натяжения
Для характеристики свойств жидкости используется величина, коэффициент поверхностного натяжения которая численно равна силе поверхностного натяжения F пна единицу длины l контура, ограничивающего поверхность жидкости:
σ = F п / l
Теперь рассмотрим случай на рис. 3 мы можем записать q=2F п=2σ l. Из этого условия можно вычислить значение коэффициента поверхностного натяжения:
σ = q /2 l
Единица измерения для коэффициента поверхностного натяжения в системе СИ — Ньютон на метр (н/м), в системе СГС — дин/см.
Зависимость поверхностного натяжения от температуры
При повышении температуры расстояние между молекулами жидкости увеличивается, а притягивающие силы соответственно уменьшаются.
Поэтому коэффициент поверхностного натяжения (особенно в случае чистых жидкостей) с повышением температуры увеличивается
Зависимость коэффициента поверхностного натяжения для воды приведены в таблице
| t°c | 0 | 20 | 50 | 100 | |
| σ | п/м | 0,0750 | 0,0725 | 0,0679 | 0,0588 |
| дин/см | 75,6 | 72,5 | 67,9 | 58,8 | |