5. расчет. \(Q_1 \) = 4200 Дж/кг — °C -0,2 кг -20°C = 16800 Дж \(Q_2 \) = 4200 Дж/кг — °C -0,1 кг -40°C = 16800 Дж
О тепловой энергии простым языком!
Человечеству известно несколько видов энергии: механическая (кинетическая и динамическая), внутренняя (тепловая), внешняя (гравитационная, электромагнитная и ядерная) и химическая. Особого упоминания заслуживает энергия взрывов.
. Вакуумная энергия и до сих пор существует только в теории — темная энергия. В этой статье, первой в рубрике «Теплотехника», мы постараемся простым, понятным языком, на практических примерах рассказать о наиболее важных в жизни человека видах энергии. Время.
Несколько слов о понимании положения теплотехники как науки о производстве, транспортировке и применении тепловой энергии. Современная теплотехника возникла из общей термодинамики — раздела физики. Термодинамика — это буквально «тепло» и «энергия». Таким образом, термодинамика — это наука об «изменении температуры» системы.
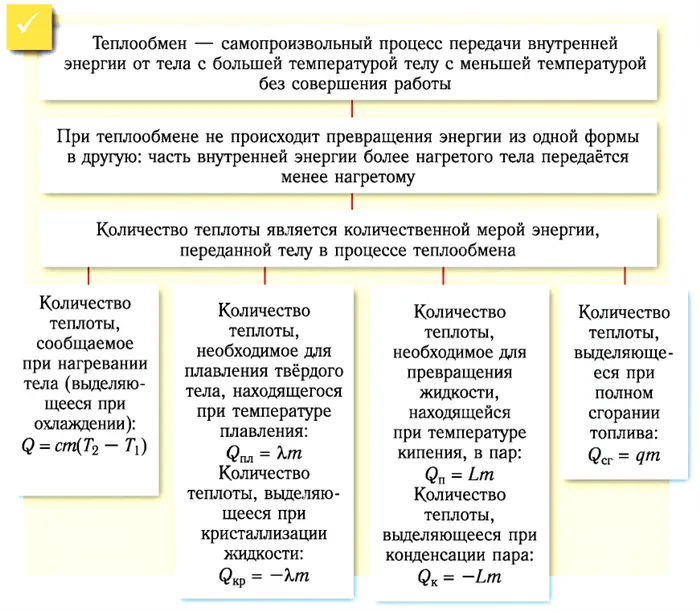
Воздействие на систему извне, изменяющее внутреннюю энергию, может быть результатом теплообмена. Тепловая энергия, полученная или потерянная системой в результате этого взаимодействия с окружающей средой, называется теплотворной способностью и измеряется в джоулях системы СИ.
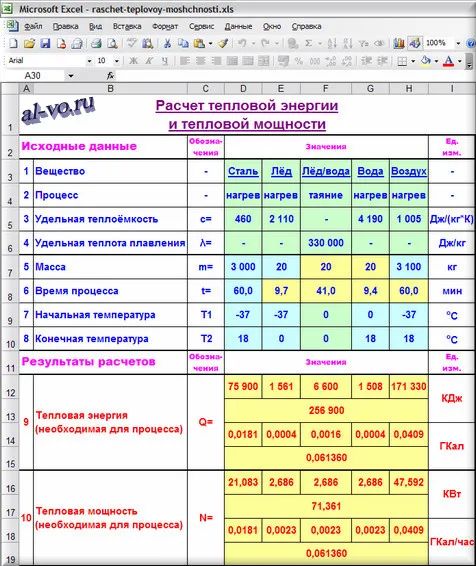
Если вы не являетесь инженером-теплотехником и не имеете дело с теплотехникой каждый день, вам может быть трудно сразу разобраться в ней, если вы не имеете опыта. Даже знание размеров измеряемого и производимого тепла может быть затруднительным без опыта. от -37°C до +18°C к количеству джоулей энергии, необходимых для нагрева 1000 кубических метров воздуха. Сколько энергии необходимо источнику тепла, чтобы сделать это за один час? Не все инженеры сегодня отвечают на эти довольно сложные вопросы «на ходу». Иногда эксперты даже помнят людей, но мало кто может их реально применить!
Прочитав эту статью до конца, вы сможете легко решать реальные производственные и бытовые проблемы, связанные с нагревом и охлаждением различных материалов. Понимание природы процесса теплопередачи и знание простых основных типов являются основными строительными блоками для фундамента знаний в области механической теплоты!
Количество теплоты при различных физических процессах.
Большинство известных веществ могут быть твердыми, влажными, газообразными или фиктивными при различных температурах и давлениях. Переход из одного когезионного состояния в другое осуществляется при постоянной температуре (если давление и другие параметры окружающей среды не изменяются) и включает в себя поглощение или выделение тепловой энергии. 99% материала во Вселенной находится в плазменном состоянии, но в данной статье эта общая ситуация не рассматривается.
Посмотрите на график на рис. Она показывает зависимость температуры T вещества от количества тепла Q, подведенного к замкнутой системе, содержащей определенную массу вещества.
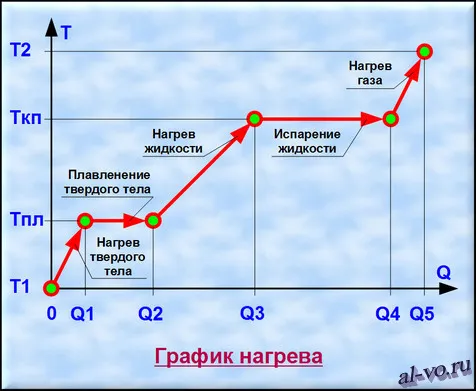
1. нагревание твердого тела при температуре T1 до температуры TP равно Q1 для данного теплового процесса.
2. затем начинается процесс плавления, который происходит при постоянной температуре TPL (температура плавления). Чтобы расплавить всю твердую массу, необходимо затратить количество тепловой энергии, равное Q2 -Q1.
3.Далее нагревается жидкость, полученная в результате плавления твердого тела при температуре кипения (образования газа) Ткп, и это количество тепла равно Q3-Q2.
4.Теперь, при определенной температуре кипения Ткп, жидкость закипает и испаряется, превращаясь в газ. Для преобразования всей массы жидкости в газ необходимо затратить тепловую энергию, равную Q4-Q3.
5. последний шаг — нагрев газа от температуры Tkp до температуры T2. В то же время количество потребляемого тепла составляет Q5-Q4. (Нагрев газа до температуры ионизации превращает газ в плазму).
Таким образом, при нагревании первого твердого тела от температуры T1 до температуры T2 было затрачено Q5 тепловой энергии, что перевело вещество в три когезионных состояния.
Двигаясь в обратном направлении, такое же количество тепла Q5 отводится от вещества, проходя стадии конденсации, кристаллизации и охлаждения от температуры T2 до температуры T1. Разумеется, рассматривается закрытая система без потерь энергии во внешнюю среду.
Обратите внимание, что можно обойти жидкую фазу и перейти из твердого состояния в газообразное. Этот процесс называется сублимацией, а обратный процесс — сушкой.
Таким образом, мы узнали, что процесс перехода между кумулятивными состояниями материи характеризуется расходом энергии при постоянной температуре. Когда вещество нагревается до неизменного кумулятивного состояния, его температура повышается, и тепловая энергия также расходуется.
Главные формулы теплопередачи.
Количество тепла от Q до J рассчитывается по следующему уравнению
1. с точки зрения потребления тепла, т.е. с точки зрения нагрузки:.
1.1 На стороне нагрева (охлаждения):.
Q = m * c * (T2-T1)
m — масса вещества (кг)
c — удельная теплоемкость вещества (Дж / (кг * К))
1.2 Сторона плавления (замораживания)
Q =m*λ
λ — удельная теплота плавления и кристаллизации вещества (Дж / кг).
1.3 Для кипения и испарения (конденсации)
Q = m * r
r — удельная теплота сгорания газа и конденсации вещества (Дж/кг).
2.2 С точки зрения производства тепла, т.е. с точки зрения источников тепла:.
2.1 в отношении сжигания топлива:.
Q = m * q
q — удельная теплота сгорания в Дж/кг.
2.2. с точки зрения преобразования электроэнергии в тепловую энергию (закон Джоуля-Ленца)
Q = t * I * U = t * R * I ^ 2 = (t / R) * U ^ 2
I — текущее значение р.м.с. A
U — значение напряжения в р.м.с. V
R — сопротивление нагрузки в омах
В заключение следует отметить, что величина теплоты прямо пропорциональна массе вещества при всех фазовых превращениях, а в случае нагревания она еще более прямо пропорциональна разности температур. Каждый коэффициент материала (c, λ, r, q) имеет свое значение, которое определяется экспериментально (берется из справочников).
Теплопроизводительность в ваттах N — это количество тепла, переданное системе в определенный момент времени.
Чем быстрее вы хотите нагреть тело до определенной температуры, тем больше мощности требует источник тепла — все логично.
Тепловые явления — это естественные процессы, происходящие в организме при его нагревании или охлаждении. Другими словами, это явления, которые происходят в организме при изменении температуры.
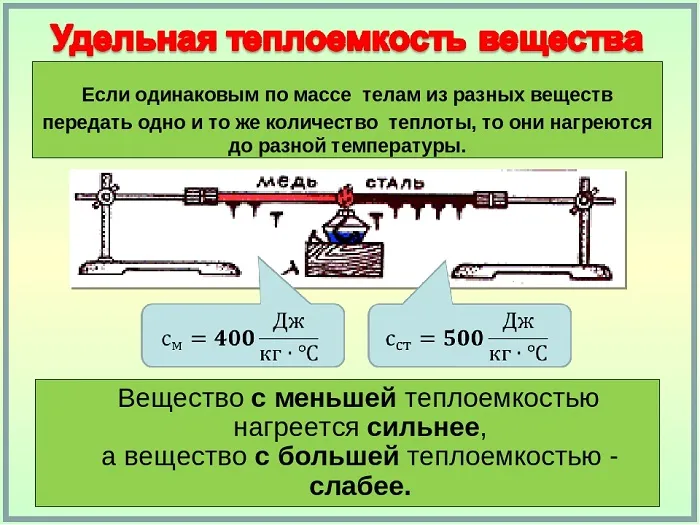
Количество теплоты. Удельная теплоёмкость

Изменение внутренней энергии в результате реализации проекта характеризуется количеством проектов. Другими словами, проект — это мера изменения внутренней энергии в конкретном процессе. Изменение внутренней энергии тела при теплопередаче характеризуется величиной, называемой количеством тепла.
Количество теплоты — это изменение внутренней энергии тела в процессе теплопередачи без совершения работы.
Количество тепла выражается в ϭ (q ϭ). Так как количество тепла является мерой изменения внутренней энергии, единицей измерения является джоуль (1 дж).
Если тело не совершает никакой работы и передает часть тепла другому телу, его внутренняя энергия увеличивается. Если тело отдает тепло, его внутренняя энергия уменьшается.
2. если две одинаковые емкости наполнить 400 г воды при той же температуре, что и 100 г воды в одной, и поставить на одну и ту же горелку, то вода в первой емкости закипит быстрее. Таким образом, чем больше масса тела, тем больше тепла требуется для его нагрева. То же самое относится и к охлаждению. Тела с большей массой выделяют больше тепла при охлаждении. Эти тела сделаны из одного и того же материала и нагреваются или охлаждаются на одинаковое количество градусов.
3 В настоящее время нагревание 100 г воды с 30 °C до 60 °C, т.е. до 30 °C, а затем до 100 °C, т.е. до 70 °C, в первом случае требует времени. При втором, соответственно, то, что необходимо для нагрева воды, меньше 30°C, чем 70°C, поэтому величина тепла прямо пропорциональна разнице между конечной ˮ((t_2 \, ^\ circ)ˮ) и начальной температурой ˮ((t_1 \, ^\ circ c)ˮ). \ sim(t_2-t_1).
4. если в один контейнер налить 100 г воды, а в другой такого же вида налить воду и металлическое тело так, чтобы его масса и масса воды составляли 100 г. Если контейнеры нагревать одинаково плитой, то контейнер, содержащий только воду, будет иметь более низкую температуру, чем контейнер, содержащий воду и металлическое тело. Поэтому, чтобы достичь температуры содержимого обоих контейнеров, необходимо передать воде больше тепла, чем воде или металлическому телу. Поэтому количество тепла, необходимое для нагревания тела, зависит от типа вещества, из которого это тело изготовлено.
5.В зависимости от количества тепла, необходимого для нагревания тела от вида вещества, характеризуется его естественная величина, называемая удельной теплоемкостью вещества.
Натуральная величина, равная количеству тепла, необходимого для нагревания 1 кг вещества на 1 °C (или 1 к) (или 1 к), называется удельной теплоемкостью.
Такое же количество теплоты при охлаждении на 1 °C выделяет 1 кг вещества.
Специальные теплоемкости обозначаются буквой ɑ (c \). Единицами измерения специальной теплоемкости являются 1 дж/кг °C или 1 дж/кг К.
Цена удельных тепловых свойств вещества определяется экспериментально. Жидкости имеют более высокую специальную теплоемкость, чем металлы. Вода обладает самой большой специальной теплоемкостью, а золото имеет очень низкую специальную теплоемкость.
ПРИМЕРЫ ЗАДАНИЙ
1. специальное серебро имеет теплоемкость 250 дж/(кг — °C). Что это значит?
1) 1 кг серебра 1 кг x количество тепла, выделяемого при охлаждении 1 j 2) 1°°C при охлаждении 250 кг серебра 1 j 3) 1°°° при охлаждении 250 кг серебра 1 j 3) Тепловая оснастка 1 j 4) 1 кг серебра 1°°° при охлаждении — выделение тепла 250 j
2. специальная теплоемкость цинка составляет 400 дж/(кг -°C). Это означает.
1) нагревание 1 кг цинка до 400 °C увеличивает его внутреннюю энергию на 1 j 2) нагревание 400 кг цинка при 1 °C увеличивает его внутреннюю энергию на 1 j 3) нагревание 400 кг цинка при 1 °C требуется 1 дж энергии 4) Нагревание 1 кг цинка при температуре 1 °C увеличивает его внутреннюю энергию на 400 дж
3. когда твердая масса ˉ (m \) переходит в твердую массу ˉ (q \), температура тела повышается на ˉ (ˉ delta t^{ circ \). Какое из следующих выражений определяет удельную теплоемкость данного вещества тела?
4.График на диаграмме показывает количество теплоты, необходимое для нагревания двух тел (1 и 2) с равными объемами, связанными с температурой. Сравните значения специальной теплоты сгорания вещества, из которого состоят два тела (⌘(c_1 \) и ⌘(c_2 \)).
1)ˉ(c_1 = c_2 \) 2)ˉ(c_1> c_2 \) 3)ˉ(c_1 4) Ответ зависит от величины массы тела
5.На диаграмме показано количество теплоты, переданное двум телам одинакового количества при изменении температуры на один и тот же градус. Какова взаимосвязь между удельной теплоемкостью тела правильного вещества?
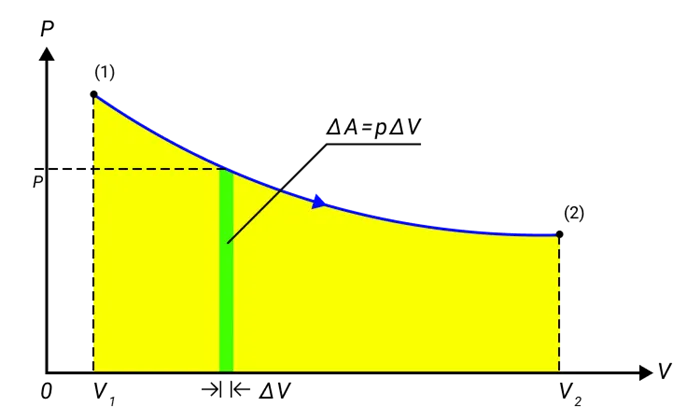
1) ˉ (c_1 = c_2 \) 2) ˉ (c_1 = 3c_2 \) 3) ˉ (c_2 = 3c_1 \) 4) ˉ (c_2 = 2c_1 \)
6.График на рисунке показывает температуру твердого тела в зависимости от количества выделяемого тепла. Масса твердого тела равна 4 кг. Какова удельная теплоемкость вещества тела?

1) 500 дж/(кг — °C) 2) 250 дж/(кг — °C) 3) 125 дж/(кг — °C) 4) 100 дж/(кг — °C)
7. температура вещества и количество теплоты, переданное веществу, были измерены при нагревании 100 г кристаллов. Данные измерений были представлены в виде таблиц. Предполагая, что потери энергии пренебрежимо малы, определяется удельная теплоемкость твердого тела.
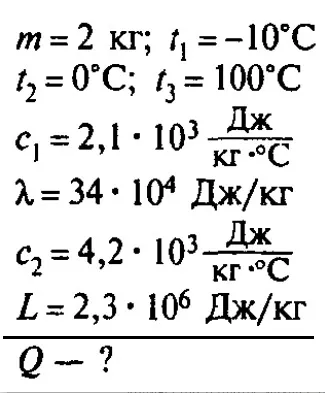
1) 192 Дж/(кг — °C) 2) 240 Дж/(кг — °C) 3) 576 Дж/(кг — °C) 4) 480 Дж/(кг — °C)
8. чтобы нагреть 192 г молибдена при 1 К, количество теплоты, переданное ему, составляет 48 Дж. Какова удельная теплоемкость этого вещества?
1) 250 дж/(кг -к) 2) 24 дж/(кг -к) 3) 4-10 -3 дж/(кг -к) 4) 0,92 дж/(кг -к)
9. какое количество теплоты требуется для нагревания 100 г свинца от 27°C до 47°C?
1) 390 J 2) 26 KJ 3) 260 J 4) 390 KJ
10. если необходимо, для нагревания кирпича от 20°C до 85°C требуется столько же тепла, сколько для нагревания воды при температуре 13°C. Теплоемкость специальных кирпичей составляет.
Часть 2
C1. 2 кг твердых веществ нагреваются в печи мощностью 2 кВт. На графике показана температура твердого тела в зависимости от времени нагрева\(\ tau \)}. Какова удельная теплоемкость вещества?
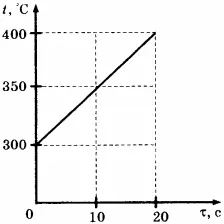
1) 400 дж/(кг°C) 2) 200 дж/(кг°C) 3) 40 дж/(кг°C) 4) 20 дж/(кг°C)
Количество тепла выражается в ϭ (q ϭ). Так как количество тепла является мерой изменения внутренней энергии, единицей измерения является джоуль (1 дж).
Обратимые и необратимые процессы
Проект численно равен площади процесса, изображенного на рисунке P, v. Значение A зависит от способа перехода из начального состояния в конечное. На рисунке 2 показаны три процесса, которые переводят газ из состояния (1) в состояние (2). Во всех случаях газ совершает работу.
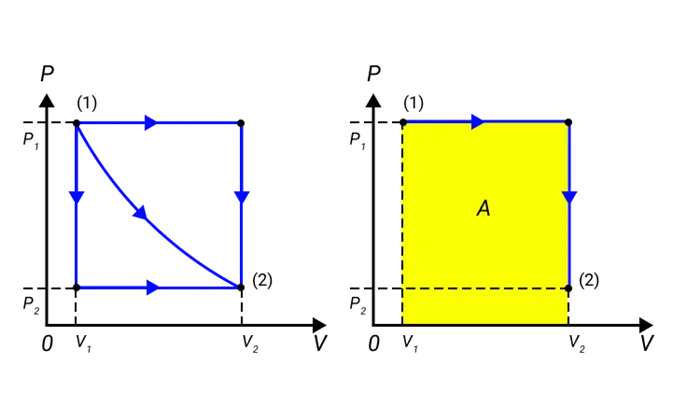
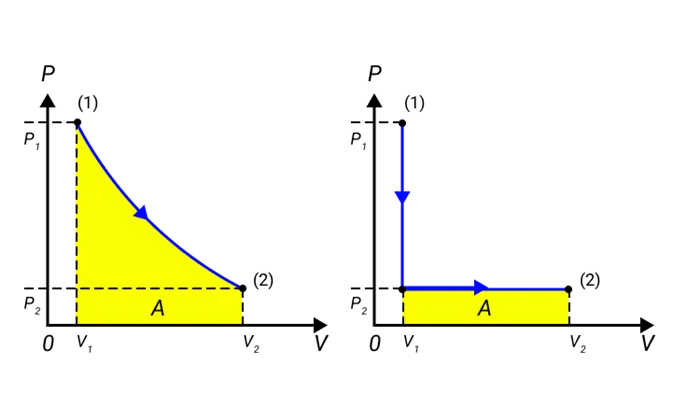
Рисунок 2: Три различных пути от состояния (1) к состоянию (2). Во всех трех случаях GAS выполняет различные проекты, равные площади под диаграммой процесса.
Процедуру на рисунке 2 можно выполнить в обратном направлении. В этом случае символ A преобразуется в обратном направлении.
Процессы, которые могут выполняться в обоих направлениях, называются реверсивными.
Жидкости и твердые частицы можно не учитывать при выполнении работы, так как их потенциальные изменения несущественны для объема. Однако их внутренняя энергия изменяется в результате работы.
Процедура разогревает компоненты. Это способствует изменению внутренней энергии. Эксперимент Джоуля, проведенный в 1843 году, является еще одним примером. Это помогает определить механический эквивалент тепла, который проявляется в повышении температуры жидкости из-за трения, т.е. потому что происходит увеличение внутренней энергии.
Поскольку процессы в примере не могут протекать в противоположных направлениях, они называются необратимыми.
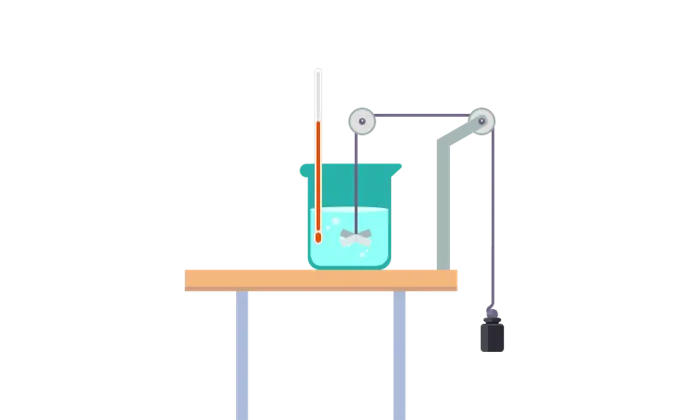
Рисунок 3: Упрощенная диаграмма эксперимента Джоуля для определения механических эквивалентов тепла.
Наличие проекта и теплообмен могут изменить внутреннюю энергию. Тепловой контакт между телами увеличивает энергию одного тела и уменьшает энергию другого. По-другому это называется тепловым потоком.
Количество теплоты
Количество тепла Q называется внутренней энергией, возникающей в результате теплообмена.
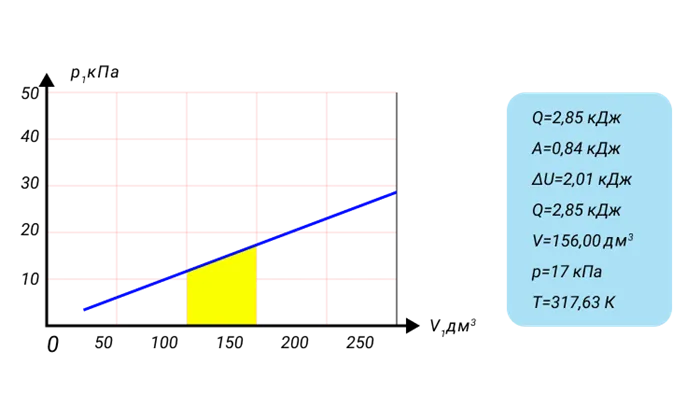
Рисунок 4: Модель газового проекта.
Процессы теплопередачи возможны только при различных температурах.
Направление теплового потока всегда направлено в сторону холодного тела.
Количество тепла Q считается энергетической величиной и измеряется в джоулях (j).
1) Зависит от вещества, из которого изготовлен цилиндр. (2) Он не зависит от вещества, из которого изготовлен цилиндр. (3) Он увеличивается с увеличением массы цилиндра. (4) Увеличивается с увеличением разницы температур. 5) Удельная теплоемкость алюминия в четыре раза больше удельной теплоемкости олова.
Удельная теплота сгорания топлива
Физическую величину, численно равную количеству теплоты, выделяющемуся при полном сгорании топлива массой 1 кг, называют удельной теплотой сгорания Количество теплоты, выделившееся при полном сгорании некоторой массы
Это количество тепла передается телам, составляющим термодинамическую систему, и является для них положительным.
Примеры решения задач
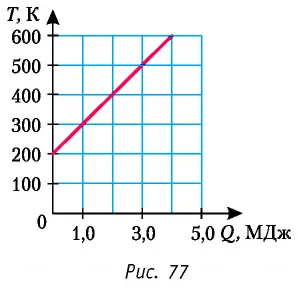
На рисунке 77 представлен график зависимости абсолютной температуры нагреваемого тела от переданного ему количества теплоты. Воспользовавшись таблицей на с. 84, определите вещество, из которого изготовлено тело, если его масса
Чтобы определить вещество, из которого изготовлены тела, найдем удельное тепловыделение c. Анализируя график, мы пришли к выводу, что когда тело нагревается до определенной температуры, оно может передавать количество тепла в зависимости от типа.
Поэтому удельная теплоемкость вещества консервируется полученным значением удельной теплоемкости.
Ответ — жесть.
В емкость, наполненную водой, добавляют немного льда при температуре, пренебрегая теплоемкостью и тепловыми потерями. Специальная теплоемкость льда Специальная теплота льда

Игнорируйте потери энергии в окружающую среду и рассматривайте только обмен энергией между телами системы. Рассмотрим тепловые процессы, происходящие в системе: 1) нагрев льда за счет температуры 2) таяние льда: 3) нагрев воды, происходящий при таянии льда за счет температуры 4) охлаждение горячей массы воды до температуры Составим уравнение теплового баланса: или

Где находится ледяная масса:.

Ответ:
Чтобы скопировать материал с сайта evkova.org, посетите www.evkova.orgへのアクティブなリンクが必要です.
Этот сайт создан группой преподавателей на некоммерческой основе для дополнительного образования молодежи.
Сайт создан, поддерживается и управляется командой учителей
Telegram и логотип Telegram являются торговыми марками TelegramCorporationFZ-LLC.
Данный веб-сайт носит исключительно информационный характер и не является публичной офертой, определяемой положениями Статьи 437 Гражданского кодекса Российской Федерации. АннаЕвкова не оказывает услуг.