-в \(⌘ бета^ — \) — исходное ядро и делится на следующие ячейки после электронов и антитринов (незаряженных частиц и остальных):.
Атомное ядро
Атомное ядро — это положительно заряженная внутренняя часть человека. Разделение человека на индивидуальное ядро и индивидуальную оболочку соответствует Эрнесту Резерфорду. Эрнест Резерфорд в своих экспериментах по рассеянию в 1911 году показал, что человек должен состоять из небольшого твердого ядра, состоящего из легких оболочек. Диаметр ядра человека в 20 000-150 000 раз больше диаметра атомной оболочки, но содержит более 99,9% массы человека. Ядро человека состоит из протонов и (за исключением одного часа) нейтронов. Атомное ядро определяет количество протонов (атомный номер, атомный номер) и, таким образом, структуру электронной оболочки, а следовательно, и количество электронов в электрически нейтральном атоме через химические свойства индивида. Протоны и нейтроны ограничены в ядре ядерными силами. Если структура или состояние ядра изменены, например, в радиоактивности B., то преобразованная энергия может быть в миллионы раз больше, чем при химии оболочки.
Отрасль физики, изучающая ядра, называется ядерной физикой. Что касается отдельных сердечников, то префикс «индивидуальный» использовался в основном в ранние годы. Позже оно было заменено латинским nucleus, прежде всего ядро или нуклеус, ядро. Термин ядро относится к чему-либо или эффекту, связанному со свойствами или реакциями отдельного ядра. Ядерная медицина .
Отдельные типы особей называются ядрами в соответствии со структурой отдельного ядра.
Об истории исследования отдельных ядер см. Ядерная физика # История.
Оглавление
Размер, плотность, компоненты, названия
Ядро человека находится, говоря простым языком, в центре человека — его диаметр составляет примерно 1 /20 000 1 / к150 000 по. диаметра электронной оболочки. Атомное ядро имеет z. B. диаметр около 1 фм (фемтометр), а небесный диаметр — около 16 фм. В зависимости от элемента, его ядро составляет 99,95-99,98 процента от общей массы.
Плотность ядра (отношение массы ядра к его объему) примерно одинакова для всех ядер и составляет от около 2 до 10 17 кг/м³. Материалы с такой плотностью называются ядерными материалами. Например, чтобы достичь такой плотности, пирамиду HEOPA пришлось сжать до размера перца.
Ядро состоит из протонов и нейтронов, которые имеют примерно одинаковую массу и вместе называются нуклонами. Число протонов называется атомным номером и обычно обозначается символом. (Общее число нуклонов называется массой, а число нейтронов обозначается символом, более подробную информацию о массе ядра см. в разделе «Масса ядра или неполная масса»). Количество людей, найденных естественным образом на Земле, колеблется от (1 ч. нормального водорода) до 244 (244 ПУ). С другой стороны, макроскопическая плотность обогащенной материи не увеличивается пропорционально индивидуальным массам, поскольку атомные радиусы также увеличиваются в среднем в 3-4 раза (см. индивидуальные радиусы, за исключением сильных циклических вариаций). Z A. N A. Синус равен Z + N A. Синус равен 1
Протоны заряжены положительно, а нейтроны — нейтрально. Поэтому атомное ядро заряжено положительно и может связывать отрицательно заряженные электроны благодаря кулоновским силам. Поскольку нагрузка электронов и протонов обратно пропорциональна, электрически нейтральный человек имеет столько же электронов в атомной оболочке, сколько протонов в ядре. Поскольку атомная оболочка в основном определяет химические свойства, атомный номер также определяет, к какому элементу принадлежит индивид.
Количество нейтронов незначительно влияет на химические свойства, но существенно для стабильности или нестабильности (радиоактивности) ядра. Помимо спонтанного радиоактивного распада, количество протонов или нейтронов в ядре может изменяться только в результате ядерных реакций. То есть в результате столкновения ядра с другим ядром или другой частицей.
Тип человека или ядра, определяемый его количеством атомов и массой, называется нуклеидом. Ядра GG включают оба масштабных ядра, ядро UU и два ядра нуклидов, а также ядро UG или GU и два линейных ядра. Если изомеры являются ядрами при определенных уровнях стимула (см. ниже), они считаются собственными ядрами. Когда мы различаем ядра (или целые ядра) одного и того же элемента, то есть с одинаковым числом протонов и по числу нейтронов, мы говорим об изотопах соответствующего элемента. Нуклеиды характеризуются химическими символами и массовыми числами. B. Наиболее распространенный изотоп углерода 12 C или наиболее распространенный изотоп железа 56 Fe (с изомерами с добавлением «переходного» типа «M»). Реже встречаются названия C-12 или FE-56 или ненужное дополнительное указание номера заказа. Z n z n 26th 56th Fe. e _ ^^ \ mathrm>
Всего известно около 3200 макробионтных нуклеидов (с 2003 года), распределенных между примерно 2700 изотопами и 118 известными элементами — от водорода до онканов. В их составе имеется около 250 постоянных изотопов. Ядерная стабильность зависит от количества протонов и нейтронов. Если эти два числа выходят за пределы определенного диапазона, то ядро нестабильно. Он радиоактивен и преобразуется в более стабильное ядро. Для протонов с номерами выше 43, 61 и 82 фиксированное ядро отсутствует.
Основные модели
В ядерной физике не существует единой модели, которая бы полностью объясняла все процессы в отдельных ядрах. По сравнению с индивидуальной физикой, где отдельные квантовомеханические модели были успешными, ядра не имеют специального центра масс, а силы между нуклонами намного сложнее, чем чисто электромагнитные взаимодействия индивидов. Поэтому для разных вопросов используются разные базовые модели. Наиболее важными из них являются следующие
- Модель капли ( Карл Фридрих фон Вейцзеккер, 1935, Нильс Бор, 1936) описывает атомное ядро как сферическую каплю электрически заряженной жидкости и дает формулу для ее полной энергии связи. С помощью этой почти классической модели легко объяснить, какие изотопы стабильны, а какие еще можно преобразовать в более прочно связанные посредством высвобождения энергии, например, посредством α-распада, β-распада, деления ядер. Это значит, в том числе. также количество стабильных химических элементов на Земле является оправданием.
- Модель оболочки для ядер ( Maria Гепперт-Майер, Дж Ханс Д. Jensen, 1949) прослеживает структуры атомных ядер по аналогии с оболочечной модели атомной физики чисто квантово — механических законов ( орбитали в потенциальной яме, принцип Паули ). Взаимодействие между двумя нуклонами рассматриваются только в дальнейшем уточнении. Оболочечная модель может объяснить отклонения от модели капли с точки зрения энергии связи ядер, в частности высокой стабильности с определенными так называемыми магическими числами протонов и нейтронов. Он также предоставляет подробные объяснения уровней энергии, ядерных спинов, магнитных моментов, механизмов ядерных реакций, поскольку они являются результатом движения одного или очень небольшого числа нуклонов в ядре. Однако часто возбужденные состояния атомного ядра образуются с участием многих или даже всех нуклонов.
- Коллективная модель ( Оге Нильс Бор, Бен Моттельсон, 1953) используется для деформированных ядер для описания коллективных возбуждений (колебаний и вращений). Эти ядра не имеют точной сферической формы, а слегка приплюснуты в одном направлении или несколько вытянуты, что видно, например, по электрическим квадрупольным моментам этих ядер. В результате получается характерная схема уровней возбужденных состояний в виде полосы колебаний или полосы вращения.
- В единой модели ( Джеймс Рейнуотер, 1957) модель оболочки и коллективная модель объединены.
Другими частично очень упрощенными моделями или моделями, которые рассматриваются для конкретных целей, являются, например, следующие
- Модель Фермигаза (также единая модель ). Здесь предполагается, что нуклоны свободно перемещаются, несмотря на их сильные взаимодействия, и подчиняются только принципу Паули. Эта идея используется в модели капли энергии связи для обоснования энергии асимметрии , которая описывает влияние отношения числа нейтронов к числу протонов.
- Модель альфа-частиц . Альфа-частицы здесь представляют собой стабильные субъединицы внутри ядра, которое z. Б. для сердечников C-12, O-16, Ne-20 дает полезное модельное представление.
- Модель потенциальной скважины . Здесь, по аналогии с атомом, задан некоторый потенциал, из которого определяется спектр естественных энергетических состояний отдельного нуклона. Это основа оболочечной модели и пространственно ограниченной модели Фермигаза. Простой коробчатый потенциал, осцилляторный потенциал и значительно более реалистичный потенциал Вудса-Саксона являются основными формами потенциала.
- Оптическая модель . Здесь ядерные реакции моделируются в том смысле, что на падающий снаряд воздействует ядро цели так же, как на световую волну воздействует поглощающая («облачная») линза. Модель хорошо подходит для упругого рассеяния, а также для реакций, в которых только частица отрывается от ядра мишени или добавляется к нему.
- Модель взаимодействующих бозонов. Здесь нуклоны вне замкнутой оболочки сначала объединяются в пары протонов или нейтронов, а на следующем этапе моделируются их взаимодействия.
Тепловой синтез может стать возможным альтернативным источником энергии. Поиск таких источников энергии важен в связи с ограниченностью запасов нефти и газа на Земле.
Масса ядра
Другой важной функцией ядра также является его масса. Индивидуальная и ядерная масса обычно выражается в индивидуальных единицах массы (A.M.U.), где индивидуальная единица массы равна 12, что составляет 1 12 массы c 6 12 углеродного ядра.
Где n a = 6, 022-10 23 м о л -1 обозначает число Авогадро.
Существует и другой способ выражения атомных величин. Она выражается в единицах энергии на основе соотношения Эйнштейна E = m c 2. Поскольку масса протона mp = 1. 00728π.μ. = 938, 28 M e V, масса нейтрона m n = 1. 00866π.μ. = 939, 57 M e V, а масса электрона m e = 5, 49.10-4a. em. = 0.511 M e V.
Из приведенных выше значений следует, что масса электрона немного меньше массы ядра. Поэтому масса ядра практически равна массе всего атома, в отличие от целого числа.
Масса ядра, выраженная в ае. м. Округленное до целого числа, оно называется массовым числом и обозначается буквой A. Характеризует количество нуклонов в ядре.
Число нейтронов в ядре соответствует N=A-Z. Для обозначения ядра используется символ XZA. Здесь X определяется как химический символ данного элемента.
Ядра с одинаковым числом протонов, но разными массовыми числами называются изотопами.
Некоторые элементы имеют десятки стабильных и нестабильных изотопов. Уран имеет 14 изотопов, от U92227 до U92240. Большинство химических элементов в природе представляют собой смеси различных изотопов. Наличие именно изотопов объясняет следующее явление: некоторые физические элементы имеют массу, отличную от целого числа. В качестве примера рассмотрим природный хлор, который состоит на 75% из C 17 35 l и на 24% из C 17 37 l и чья атомная масса соответствует 35, 5a. е. м. Для большинства атомов изотопы имеют примерно одинаковые физические и химические свойства, за исключением водорода. Однако, помимо чисто ядерных свойств, изотопы существенно отличаются друг от друга. Некоторые из них являются стабильными изотопами, другие — радиоактивными.
Ядра с одинаковыми массовыми числами, но разными значениями Z называются равновесными (например, A 18 40 r, C 20 40 a).
Ядра с одинаковым числом нейтронов определяются как изотопы.
Среди легких ядер есть пары так называемых «зеркальных» ядер. Это пары ядер с чередующимися номерами Z и A-Z. Примерами таких ядер являются C613 и N713 или H13 и H23e.
Размер атомного ядра
Как только принято, что ядра имеют почти сферическую форму, появляется возможность ввести понятие радиуса R. Обратите внимание, что для некоторых ядер наблюдается небольшое отклонение от симметрии распределения заряда. Кроме того, ядра являются динамическими, а не статическими системами, и понятие радиуса ядра не может быть выражено как радиус сферы. В связи с этим размер ядра следует рассматривать как область, в которой действуют ядерные силы. При разработке количественной теории рассеяния α-частиц Э. Резерфорд предположил, что ядра и α-частицы взаимодействуют по закону Кулона, т.е. электрическое поле вокруг ядра сферически симметрично.
Это работает для альфа-частиц с гораздо меньшими значениями энергии E. В этом случае частица не может преодолеть кулоновский потенциальный барьер и не достигает области, где действуют ядерные силы. Частица α достигает этого предела, как только энергия частицы увеличивается до определенного предельного значения Er. В таких случаях рассеяние частицы a приводит к отклонению от формулы Резерфорда.
Экспериментально известно, что радиус R ядра зависит от числа нуклонов в составе ядра.
Размер ядра определяется экспериментально путем рассеяния протонов, быстрых нейтронов или высокоэнергетических электронов. Также доступен список других косвенных методов получения значений размера ядра. Они основаны на:.
- на связи времени жизни α — радиоактивных ядер с энергией выпущенных ими α — частиц;
- на оптических свойствах, носящих название мезоатомов, в которых один из электронов временно захвачен мюоном;
- на сравнении энергий связи парных зеркальных атомов.
Эти методы подтверждают эмпирическую зависимость R = R 0 A 1/3, и значения констант R 0 = 1, 2 -1 и 5-10-15m также определяются с помощью таких измерений. Отметим также, что единицы расстояния в атомной физике и физике частиц считаются единицами Ферми, равными 10-15 м 1 f =10-15м. Радиусы ядер определяются их массовым числом и находятся в диапазоне 2-10-15-10-14 м. Выражение R0 из уравнения R = R 0 A1/3 и запись его в виде 4πR33 A = c o n s t показывает, что объем каждого нуклона примерно одинаков. Из этого можно сделать вывод, что плотность ядерной материи также примерно одинакова для всех ядер. На самом деле, плотность ядерной материи довольно высока. Это основано на поведении ядерных сил.
Энергия связи. Дефект масс ядер
Величина Δm, определяющая разницу между массами нуклонов, входящих в состав ядра, и массой ядра, называется дефицитом ядерной массы.
Важную информацию о природе нуклонов можно получить из закона сохранения энергии и закона пропорциональности между массой и энергией, даже не зная деталей взаимодействия между нуклонами. При изменении массы Δm соответственно изменяется энергия ΔE (.E =Δmc2), так что при образовании нуклонов выделяется определенное количество энергии. Из закона сохранения энергии можно сделать вывод, что точно такое же количество энергии требуется для расщепления нуклона на его составляющие, т.е. для удаления нуклонов друг от друга на расстояние, на котором они не взаимодействуют. Эта энергия определяется как энергия связи ядра.
Обратите внимание, что использование этой формулы довольно неудобно, поскольку в таблице указаны массы, относящиеся к массам нейтральных атомов, а не к массам нуклонов. Поэтому, чтобы облегчить расчет, формула преобразуется так, чтобы включать массу ядра вместо массы атома. Для этого массы электронов Z (m e) складываются и вычитаются в правой части уравнения. В этом случае E c in = Z m p + m e + A —Z m n —m i + Z m e c 2 = Z m H 1 1 + A —Z m n —m a c 2 — масса атома водорода, ma — масса атома.
В ядерной физике энергия часто выражается в мегаэлектронвольтах (М э В). Что касается практического применения ядерной энергии, то она измеряется в джоулях. При сравнении энергии двух ядер используется единица массы энергии, т.е. отношение массы к энергии (E = m c 2 ). Единица массы энергии (l e) равна энергии, которая соответствует массе a. м. 931, что соответствует 502 МэВ.
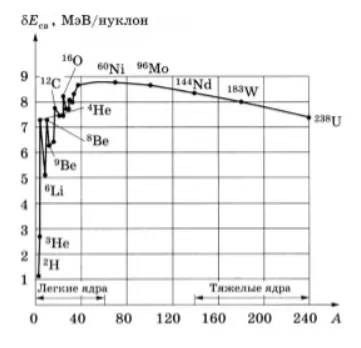
Помимо энергии, важна удельная энергия связи ядра (энергия связи на нуклон): ω = E cin/A. Она меняется относительно медленно по сравнению с изменениями массового числа A. Это объясняется тем, что он почти постоянно равен 8. 6 Me V в центральной части периодической таблицы и уменьшается к ее краю.