С увеличением числа элементарных элементов электроны имеют тенденцию к увеличению, а в подгруппах — к уменьшению. Самые низкие значения электроотрицательности характерны для первого элемента в первой группе, а самые высокие — для элемента P в седьмой группе.
Периодичность свойств элементов
Все характеристики элементов, определяемые электронной оболочкой индивидуума, закономерно изменяются в циклах и группах циклических систем. Однако, поскольку многие элементы сходных электронных структур не идентичны и сходны только при переходе от одного элемента к другому элементу подгруппы, то не происходит простого повторения свойств, а происходят более или менее интенсивные периодические изменения свойств элемента.
Химические свойства элемента определяются его способностью отдавать или добавлять электроны. Количественно это определяется энергией ионизации, сродством к электрону и электронами и зависит от радиуса индивидуума.
Атомные и ионные радиусы
Вследствие волнообразного характера движения электронов невозможно измерить абсолютный размер индивида, так как не существует его определенного предела.
Концепция орбитальных лучей недавно была расширена. Радиус орбиты — это самое удаленное от ядра расстояние наибольшего распределения электронной плотности. Таким образом, человек в базовом состоянии может иметь только лоток торговца и лоток стимулированного состояния — многие значения rПули.. На практике мы имеем дело с лучами людей, связанных определенной химической связью. Этот радиус рассматривается как фактический радиус индивида, т.е. как выявленный в результате действия. Фактический луч определяется при изучении молекулярных и кристаллических структур.
По этой причине значения атомных лучей, приведенные в различных справочниках, иногда могут значительно отличаться. Однако, несмотря на различия в значениях отдельных лучей одного и того же элемента, общая закономерность сохраняется. Это отражает зависимость атомных лучей от ядерной загрузки Z с периодическими свойствами.
Зависимость орбитальных лучей элемента r (1 Å = 10-10 м) от числа Z:.
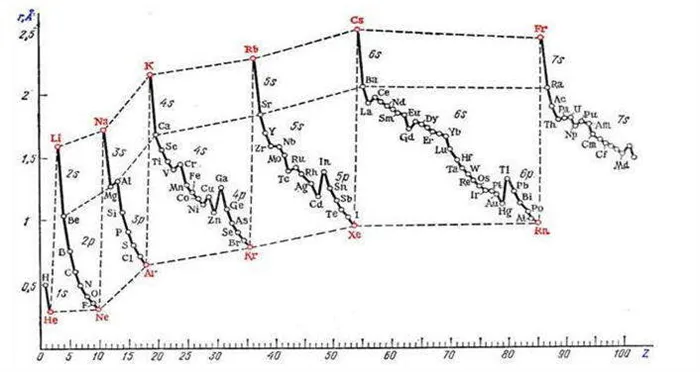
В этот же период наблюдается тенденция к уменьшению размеров особей по мере увеличения Z. Это объясняется притяжением электронов внешнего слоя к увеличению в ядре при увеличении нагрузки.
За последний период атомное излучение увеличилось, поскольку строительство новых энергетических уровней начинается дальше ядра. В результате, в пределах первичных подгрупп размер особей увеличивается с ростом ядерной нагрузки. Во вторичных подгруппах, особенно в четверговой и шестой переходных подгруппах d-металлов, размер особей изменяется в меньшей степени. Отдельные лучи почти не отличаются друг от друга. Это можно объяснить тем, что увеличение количества лучей относительно увеличения количества квантовых уровней при переходе от четвергового к шестому периоду компенсируется сокращением количества лантанидов (57ла до71Lu), вызванное заполнением уровня 4F. По этой причине элементы D пятого и шестого периодов имеют особенно схожие характеристики. Так, в подгруппе IIIB (TI-ZR-HF) последние два элемента имеют одинаковые лучи (0,145 нм) и поэтому похожи друг на друга по природным и химическим свойствам, существенно отличаясь от Титана, радиус которого составляет 0,132 нм.
Потеря атомом электронов приводит к уменьшению его фактического размера, а добавление избыточного количества электронов — к увеличению. Таким образом, радиус положительно заряженных ионов (катионов) всегда меньше, а радиус отрицательно заряженных ионов (анионов) всегда больше, чем радиус соответствующих электрически нейтральных атомов. Так, радиус атома калия составляет 0,236 нм, радиус иона калия K+ — 0,133 нм, радиус атома хлора и иона хлора SD — 0,099 нм и 0,181 нм соответственно.
Таким образом, радиус иона отличается от радиуса электрически нейтрального атома в той степени, в которой ион имеет больший заряд. Например, атомные радиусы хрома и ионов Cr2+ и Cr3+ составляют 0,127, 0,083 и 0,064 нм соответственно.
Внутри подгрупп лучи ионов с одинаковым зарядом увеличиваются с ростом заряда ядра. Эта закономерность объясняется увеличением числа электронных слоев и расстояния внешних электронов от ядра.
Энергия ионизации
Поскольку удаление электронов из невозбужденного атома и преобразование их в положительно заряженные ионы всегда является внутренним процессом (т.е. путем поглощения энергии), то для того, чтобы это произошло, необходимо выполнить какое-то действие.
Минимальная энергия, необходимая для отрыва электрона от невозбужденного атома, называется энергией ионизации I
где E и E + обозначают соответственно нейтральный атом и положительно заряженный ион (катион) элемента, I — энергия ионизации, ē — электрон.
Энергия ионизации измеряется в кДж/моль или эВ/атом. 1 эВ (электронвольт) — это энергия, получаемая электроном в ускоряющем электрическом поле с разностью потенциалов 1 В (1 эВ = 1,6-10-19 Дж) при пересчете на 1 моль, что составляет 96,5 кДж/моль. Энергия ионизации может быть определена путем столкновения электронов, ускоренных в электрическом поле, с атомом.
Один, два или более электронов могут быть отсоединены от человека с большим количеством электронов. Отсоединение каждого электрона соответствует определенному значению энергии ионизации i1, i2, …, In так что это всегда я.1 2 <… n По мере увеличения числа отделенных электронов положительный заряд иона увеличивается. Внешние электроны отделяются от атома очень легко, поскольку они обладают большей энергией, чем электроны предыдущего уровня, и для их отделения требуется относительно небольшое количество энергии. Однако при переходе к внутреннему электронному слою энергия ионизации быстро возрастает. Поэтому полностью заряженные энергетические уровни указывают на повышенную стабильность.
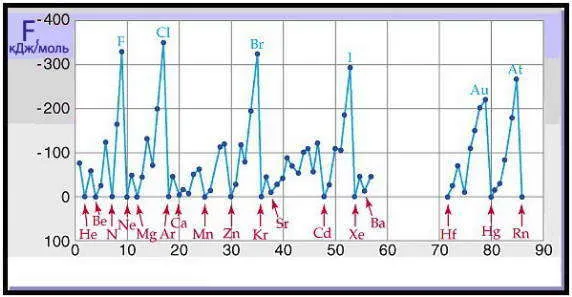
Энергия ионизации зависит от величины ядерного заряда, расстояния между ядром и внешними электронами, эффекта классификации внутреннего электронного слоя и электронной конфигурации атома. В целом можно сказать, что значение энергии ионизации зависит от положения элемента в периодической таблице и изменяется как внутри группы, так и в течение периода. Энергия десорбции первого электрона из атома периодически изменяется в зависимости от порядкового номера элемента.
Зависимость первой динамической ионизации I1 лица с номером заказа Z товара:.
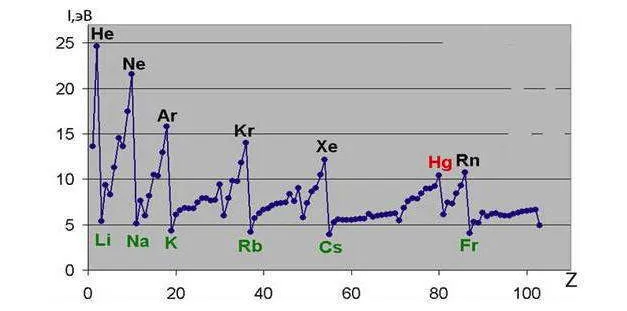
Для элементов одинаковой длительности переход от щелочных металлов к благородным увеличивает ядерную нагрузку и уменьшает лучи человека. В результате энергия ионизации постепенно увеличивается, а металлические свойства ослабевают. Однако общая тенденция к увеличению энергии ионизации в течение периода в некоторых случаях прерывается. Например, ионизирующее действие vet выше, чем ионизирующее действие B после этого; аналогичное явление наблюдается при переходе от Mg к Al, и P к повышенным значениям на полностью структурированном внешнем уровне s человека. (be, mg) или в половине точно структурированных лиц p-подуровня (n, p). Это одно из доказательств утверждения, согласно электронной конфигурации с полностью (S 2, p 6, d 10) и в равной степени полуструктурированными (p 3, d 5) подуровнями.
Энергии ионизации в последовательности d-листа немного отличаются. Это объясняется тем, что увеличение груза ядра компенсируется активностью сортирующих электронов, размещенных на внутренних энергетических уровнях.
Периодическая система химических элементов является естественной классификацией химических веществ и представляет собой периодический закон фотографа Д. Менделеева. Таблица состоит из периодов (горизонтальные линии) и групп (вертикальные колонки).
Усиление металлических и неметаллических свойств в таблице
Периодические картины Дмитрия Ивановича Менделеева очень полезны и универсальны в использовании. На основании этого можно определить определенные свойства элементов и, что самое удивительное, предсказать некоторые свойства неизученных и неизученных химическими учеными элементов (например, знать определенные свойства предполагаемых небингвистических, но еще не открытых синтезов).
Эти свойства зависят от способности элемента отдавать или притягивать к себе электроны. Важно помнить о правилах. Металлы отдают электроны, а неметаллы принимают электроны. Следовательно, металлическое свойство — это способность конкретного химического вещества отдавать свои электроны (из внешнего электронного облака) другому химическому элементу. Для неметаллов действует прямо противоположный случай. Чем легче неметалл принимает электроны, тем выше его неметаллические свойства.
Металлы не принимают электроны от другого химического элемента. Это характерно для следующих элементов.
В неметаллах положение дел аналогично. Фторид проявляет свои свойства больше, чем все другие неметаллические элементы, и может притягивать к себе частицы другого элемента, но никогда не отдает свои собственные. Он обладает самыми высокими неметаллическими свойствами. Кислород (с его характеристиками) идет сразу после фтора. Кислород может образовывать соединения с фтором, отдавая свои электроны, но при этом он забирает отрицательные частицы у других элементов.
Список неметаллических металлов с наиболее интенсивными свойствами:.
Неметаллические и металлические свойства объясняются тем, что все химические вещества стремятся к завершению своих энергетических уровней. Чтобы это произошло, для последнего уровня электронов необходимо восемь электронов. У фторида семь электронов в последней электронной оболочке, и когда он пытается ее заполнить, он притягивает еще один электрон. Натрий приобретает восемь электронов во внешней оболочке; легче отдать один, и на последнем уровне находятся восемь отрицательно заряженных частиц.
Благородные вещества не взаимодействуют с другими веществами именно из-за своего интегрального энергетического уровня. Им не нужно притягивать электроны.
Как изменяются металлические свойства в периодической системе
Регулярная таблица Менделеева состоит из групп и периодов. Периоды расположены горизонтально и включают литий, бериллий, бор, углерод, азот и кислород. Химикаты расположены в строго возрастающем порядке.
Группы расположены по вертикали, первая группа содержит литий, натрий, калий, медь, медь, серебро и т.д. Номер группы указывает на количество отрицательных частиц на внешнем уровне конкретного химического вещества. Номер периода, с другой стороны, указывает на количество электронов в облаке.
Металлические свойства непрерывно увеличиваются справа налево или, наоборот, уменьшаются в течение определенного периода времени. Другими словами, магний обладает большими металлическими свойствами, чем алюминий, но меньшими, чем натрий. Это связано с тем, что количество электронов на внешней оболочке в любой момент времени увеличивается, что усложняет процесс отдачи электронов химическим веществом.
В одной группе происходит обратное, но металлические свойства последовательно усиливаются сверху вниз. Например, калий сильнее меди, но слабее натрия. Объяснение довольно простое: число электронных оболочек в группе увеличивается, и чем дальше электроны находятся от ядра, тем легче элементу его отдать. Сила притяжения между ядром индивида и электронами первой оболочки больше, чем между ядром и электронами четвертой оболочки.
Сравните два элемента — кальций и барий. В системе журналов барий занимает более низкое место, чем кальций. Это означает, что электроны во внешней оболочке кальция находятся ближе к электронам бария, потому что они ближе к ядру.
Сравнивать элементы, принадлежащие к разным группам и периодам, сложнее. Возьмем, к примеру, кальций и лубид. Смазочные материалы выделяют отрицательные частицы лучше, чем кальций. Потому что они ниже и левее. Однако невозможно четко ответить на этот вопрос, сравнивая магний и скандий, используя только таблицу Менделеева (потому что один элемент находится ниже, а другой выше и левее). Для сравнения этих элементов требуются специальные таблицы (например, электрохимический порядок тенденций металлов).
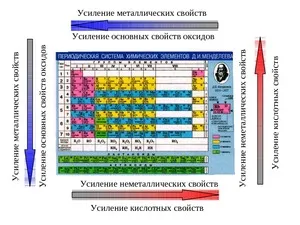
Как изменяются неметаллические свойства в периодической системе
Неметаллические свойства журнала Менделеева изменяются прямо противоположно металлическим. Фактически, эти две функции конкурируют.
Неметаллические свойства усиливаются с течением времени (непрерывно справа налево). Например, сера с меньшей вероятностью притягивает электроны хлора, но с большей, чем фосфор. Объяснение этому явлению одно и то же. Количество отрицательно заряженных частиц во внешнем слое увеличивается, что облегчает завершение энергетического уровня элемента.
Неметаллические свойства уменьшаются по очереди сверху вниз (группа). Например, фосфор может обеспечить больше отрицательно заряженных частиц, чем азот, но также лучше, чем самцы. Частицы фосфора притягиваются к ядру лучше, чем мужские частицы, что дает им преимущество быть окислительным фактором в реакциях, снижающих и повышающих степень окисления (красноватая реакция).
Сравните, например, серу и мышьяк. Сера находится выше и правее. Это означает, что сера, скорее всего, будет способствовать повышению уровня энергии. Как и в случае с металлами, неметаллы трудно сравнивать, если они принадлежат к разным группам или периодам. Например, хлор и кислород. Один из этих элементов находится выше и левее, другой — ниже и правее. Чтобы ответить на этот вопрос, необходимо обратиться к таблице электроотрицательности неметаллов. Из этой таблицы видно, что кислород легче притягивает отрицательные частицы, чем хлор.
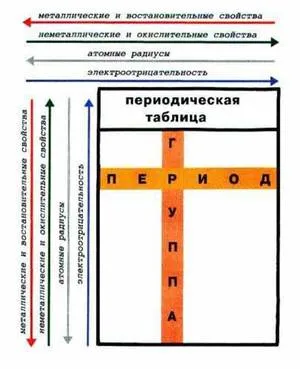
Периодическая таблица Менделеева помогает определить свойства элемента, а также узнать количество протонов в атоме, его атомный вес и атомный номер.
Способность атома отдавать электроны увеличивается с увеличением атомного радиуса, в то время как его способность принимать электроны уменьшается. Таким образом, металлические свойства увеличиваются от вершины к низу группы.
Группы (вертикальные столбцы)
Группа — это вертикальный ряд элементов, расположенных в порядке возрастания ядерного заряда и имеющих одинаковую электронную конфигурацию для внешних энергетических уровней.
В краткосрочной версии периодической таблицы есть восемь групп. Они делятся на подгруппы A (мажорные) и B (минорные). Главная подгруппа содержит элементы s и p. Подгруппы содержат d и f элементов.
Для длинных вариантов периодической таблицы существует 18 групп. Они называются так же, как и краткосрочные версии, или просто по номеру от 1 до 18 (например, группа IA или 1, VIIB или 17).
- увеличивается число электронов на последнем ЭУ (от 1 до 8);
- число ЭУ не изменяется;
- радиусы атомов в целом уменьшаются;
- электроотрицательность (способность атома в соединении удерживать электроны) увеличивается;
- металлические и восстановительные свойства простых веществ ослабевают;
- неметаллические и окислительные свойства простых веществ усиливаются;
- основные свойства оксидов и гидроксидов ослабевают;
- кислотные свойства оксидов и гидроксидов усиливаются.
Примеры работы с периодической системой
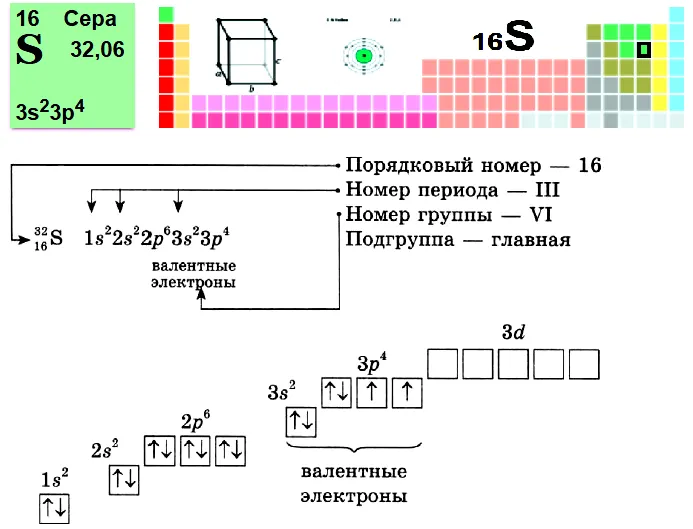
Пример № 1. сера.
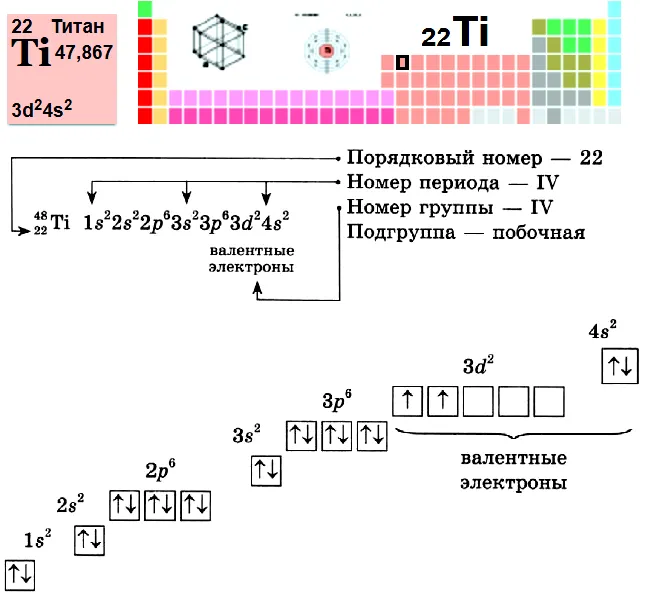
Пример № 2. титан.
Периодическое изменение свойств элементов и их соединений (наглядно)
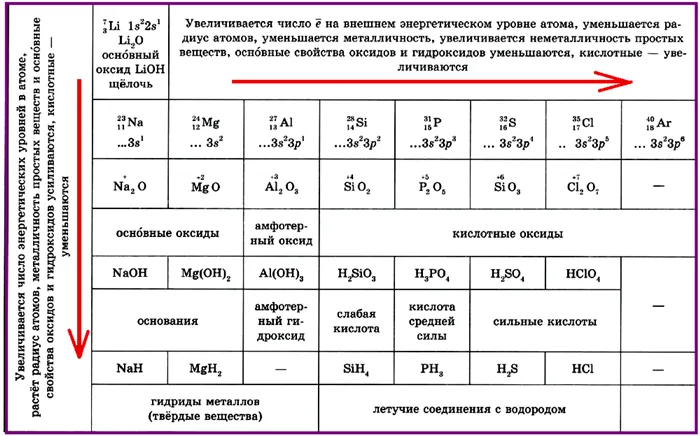
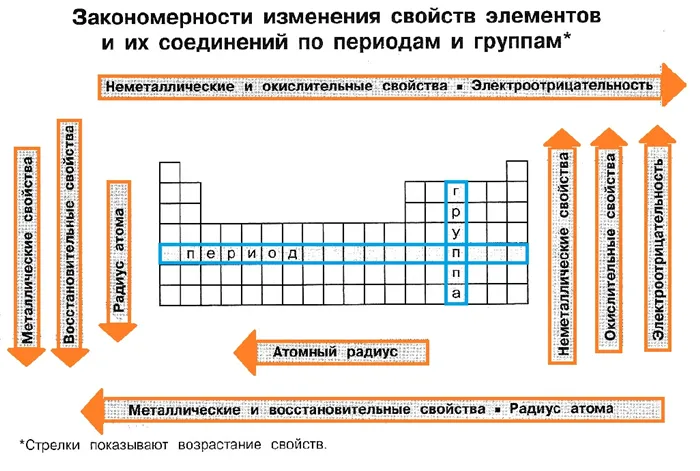
Деление элементов на металлы и неметаллы.
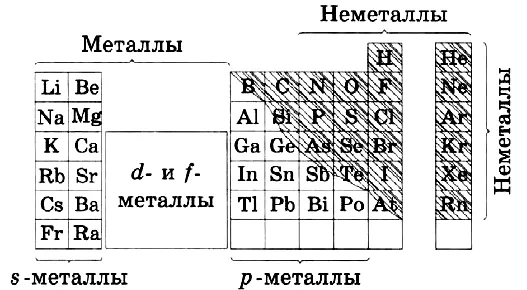
Нет четких ограничений. Некоторые элементы обладают свойствами перехода.
(c) Используются отрывки из учебников: «Химия» / Н.Е.-Москва, Эксмор (ЕГЭ. Экспресс-подготовка)» и «Химия: новый полный справочник для подготовки к ЕГЭ/Е.В.». Савинкина. -Москва, Издательство АСТ.
Рассматривали ли вы «Законы изменения свойств элементов и их соотношение по периодам и группам»? Выберите дальнейшие действия.
Преподавая химию, Менделеев обнаружил, что его ученикам трудно запомнить индивидуальные свойства каждого элемента. Он начал искать способы создания систематического способа облегчения запоминания свойств данных. В результате появились физические таблицы, которые позже были переименованы в периодические таблицы.
Фактчек
- Таблица Менделеева состоит из «столбцов», т.е. групп и «строк», т.е. периодов;
- Металлические свойства связаны со способностью отдавать электроны;
- Радиус атома увеличивается при увеличении числа электронных оболочек;
- Высшая валентность для большинства элементов равна номеру группы.
Задача 1.Какова максимальная прочность алюминия?
(Задание 2: Какое соединение водорода обладает наивысшими основными свойствами какого элемента?
(Задание 3: Из перечисленных элементов металлами являются
Задание 4: Какие элементы обладают наивысшими основными свойствами гидроксидов?
Ответ: 1. -3; 2.-1; 3.-2; 4.-3.








