Эфир или уксусная кислота — это слабая карбоновая кислота, широко используемая в промышленности. Химические свойства уксусной кислоты определяются карбоксильной группой COOH.
Уксусная кислота
Уксусная кислота (также называемая метилкарбоновой или этанолевой кислотой) встречается в виде ацетат-ионов. Именно уксус и является главным виновником кислого вкуса и запаха. Его мужчина — Ч.3 -COOH (c2 h4 o2 ). Согласно ИЮПАК, в систематическом виде она называется этаноиновой кислотой.
Это вторая простейшая карбоновая кислота после АНТ или метаномасляной кислоты и до кислоты Коуча, которая имеет только один углерод и уже имеет три цепи карбоновых кислот.
В водном растворе он может терять протон карбоксильной группы, давая основания уксусной кислоты. Его ПКА составляет 4,8 при 25°C. Это означает, что при умеренно кислом pH половина молекулы отщепляется от протона. Это делает кислоту слабее, и при нужной концентрации она может образовать регулирующий раствор с сопряженным основанием. Константа распада при 20°C Ka = 1,75-10 -5.
Интересен в органической химии как реагент, в неорганической химии как лиганд и в биохимии как метаболит (активируется как ацетил CO-Anex). Он также используется в качестве эффективной формы субстрата в реакциях, катализируемых ферментами, известными как ацетилтрансферазы, в частности, ацетилтрансферазами.
В настоящее время естественным способом его получения является карбонат метанола (реакция с CO). В прошлом его получали путем окисления этиленом ацетальдегида, который впоследствии окислялся для производства уксусной кислоты.
- В пчеловодстве он используется для борьбы с личинками и яйцами восковой моли, болезнью, называемой галериозом, которая разрушает восковые соты, которые медоносные пчелы используют для выращивания или накопления меда .
- Его применение в химической промышленности тесно связано с его сложными эфирами, такими как винилацетат или ацетат целлюлозы (основа для производства нейлона, вискозы, целлофана и т. д .).
- Широко известны его свойства в качестве протравы в фиксирующих растворах для сохранения тканей ( гистология ), где он эмпирически действует как фиксатор для нуклеопротеидов, а не для белков плазмы, глобулярных или волокнистых. (Результаты одобрены Дж. Бейкером).
- При проявлении черно-белых фотографий применялся и используется в очень слабом растворе в качестве «стоп-ванны»: при погружении в него проявляемого материала щелочность проявочной ванны нейтрализуется и процесс останавливается; впоследствии фиксирующая ванна устранила остальную часть невыявленного материала. В свою очередь, фиксаторы, которые в основном используют тиосульфат натрия в качестве основного компонента, включают уксусную кислоту в качестве подкислителя ( кислотный фиксатор ), чтобы поддерживать рН раствора достаточно низким по сравнению с раствором проявителя .
- Ацетат целлюлозы, благодаря своим качествам прозрачности и гибкости, также используется в качестве одного из основных или вспомогательных материалов для изготовления кино- и фотопленок, на которые наносится светочувствительная эмульсия. Некоторое время он также использовался в качестве подложки или основы для изготовления магнитной ленты, хотя в этом случае его успешно заменили полиэстером .
- Другое применение в медицине — в качестве красителя при кольпоскопии для выявления папилломавирусной инфекции человека, когдаткань шейки матки окрашивается в белый цвет уксусной кислотой, это положительный результат на папилломавирусную инфекцию человека, известный как положительный белый ацетат.
Его также смешивают с алкоголем, что помогает предотвратить наружный отит.
- Он также хорошо подходит для точечной уборки в целом.
- Он также используется на кухне в качестве уксуса, а также для очистки.
- В радиологии процессоры, которые проявляют рентгенографические пластины, используют ванну с уксусной кислотой, чтобы остановить процесс проявления, из которого берется рентгенографическая пластина.
Пары кислоты раздражают слизистые оболочки верхних дыхательных путей. Предел запаха уксусной кислоты в воздухе составляет приблизительно 0,4 мг/л. ПДК в воздухе окружающей среды составляет 0,06 мг/м³, а в воздухе на рабочем месте — 5 мг/м³. 4
История уксусной кислоты, структура, свойства, производство, использование
Уксусная кислота — это бесцветная органическая жидкость с химическим типом CH3ку-ку. При растворении в воде получается хорошо известная смесь под названием уксус, который издавна используется в качестве пищевой добавки. Уксус представляет собой водный раствор уксусной кислоты с концентрацией около 5%.
Как следует из названия, это кислотное соединение, поэтому значение pH уксуса меньше 7. В присутствии своих ацетатов он образует эффективную регулирующую систему для регулирования pH в диапазоне от 2,76 до 6,76. На этом этапе pH поддерживается до тех пор, пока не будет умеренно добавлено основание или кислота.

Достаточно понять, что тип образуется при соединении метильных групп (CH3) и карбоксильные группы (COOH). После муравьиной HCOOH является одной из простейших органических кислот, и это также конечная точка многих процессов ферментации.
Таким образом, уксусная кислота может быть получена путем аэробной и анаэробной бактериальной ферментации и химического состава, причем основным методом производства является процесс карбонизации метанола.
Помимо ежедневного использования в качестве заправки для салатов, в промышленности он является сырьем для производства ацетата целлюлозы — полимера, используемого в производстве фотопленки. Кроме того, уксусная кислота используется в составе поливинилацетата, который применяется в производстве клея для дерева.
Когда уксус становится слишком концентрированным, его называют уже не так, а ледяной уксусной кислотой. При таких концентрациях он является слабой кислотой, но очень едким и может вызвать раздражение кожи и дыхательных путей только при неглубоком вдыхании. Замерзающая уксусная кислота используется в качестве растворителя в органических композициях.
- 1 История
- 1.1 1800
- 1.2 1900
- 3.1 Химические названия
- 3.2 Молекулярная формула
- 3.3 Внешний вид
- 3.4 Запах
- 3.5 Вкус
- 3.6 Точка кипения
- 3.7 Точка плавления
- 3.8 Температура вспышки
- 3.9 Растворимость в воде
- 3.10 Растворимость в органических растворителях
- 3.11 Плотность
- 3.12 Плотность паров
- 3.13 Давление пара
- 3.14 Разложение
- 3.15 Вязкость
- 3.16 Коррозионная активность
- 3.17 Теплота сгорания
- 3.18 Тепло испарения
- 3.19 pH
- 3.20 Поверхностное натяжение
- 3,21 пКа
- 3.22 Химические реакции
- 4.1 Окислительная или аэробная ферментация
- 4.2 Анаэробная ферментация
- 4.3 Карбонилирование метанола
- 4.4 Окисление ацетальдегида
- 5.1 Промышленный
- 5.2 В качестве растворителя
- 5.3 Врачи
- 5.4 В еду
История.
Люди из многих культур использовали ферментацию многих фруктов, бобовых, зерна Для производства спиртных напитков и т.д. используются продукты преобразования сахаров, таких как глюкоза, в этанол, CH3CH2Огайо.
Уксус был создан по ошибке, возможно, потому что первоначальным методом производства спирта и уксуса было брожение, а возможно, из-за попыток производства спирта в неопределенное время много веков назад. Обратите внимание на сходство химических формул уксусной кислоты и этанола.
Еще в третьем веке до нашей эры греческий философ Теофраст описал действие уксуса на металлы для получения пигментов, таких как свинцовые белила.
1800
В 1823 году в Германии был разработан аппарат башенного типа для аэробного брожения различных продуктов с целью получения уксусной кислоты в виде уксуса.
В 1846 году Герман Фольбе осуществил первый синтез уксусной кислоты с использованием неорганических соединений. Синтез был начат хлорированием дисульфида углерода и завершен после двух реакций электролитическим восстановлением в уксусной кислоте.
В конце XIX — начале XX века благодаря работе Дж. Виземана бактерию Clostridium acetobutylicum начали использовать для получения уксусной кислоты путем анаэробной ферментации.
1900
В начале 20-го века преобладающей технологией было производство уксусной кислоты путем окисления ацетальдегида.
В 1925 году Генри Дрейфус из британской компании Celanese разработал экспериментальную установку для карбонилирования метанола. Позднее, в 1963 году, немецкая компания BASF предложила использовать кобальт в качестве катализатора.
ОттоХроматка и ГенрихЭбнер (1949) разработали резервуар с перемешиванием и подачей воздуха для аэробной ферментации для производства уксуса. Этот прибор до сих пор используется с некоторыми изменениями.
В 1970 году североамериканская компания Montsanto использовала систему катализаторов на основе родия для карбонилирования метанола.
Позже, в 1990 году, компания BP представила метод Катива с использованием иридиевых катализаторов для той же цели. Этот метод оказался более эффективным и менее экологичным, чем метод Монсанто.
Структура уксусной кислоты
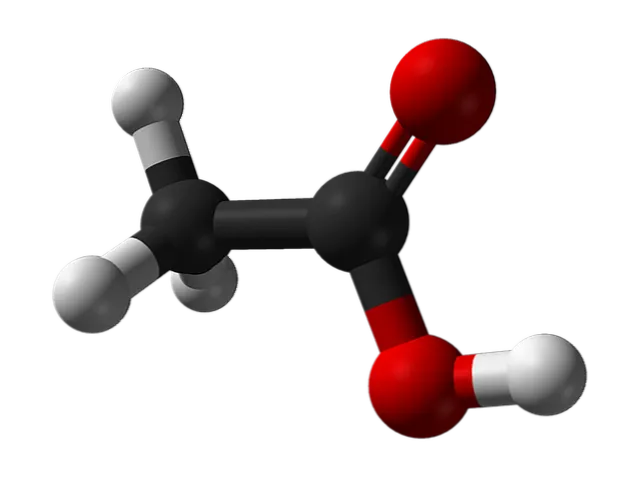
Структура уксусной кислоты, представленная моделью сферы и столба, показана на рисунке выше. Красная сфера соответствует атому кислорода, который относится к карбоксильной группе -COOH. Таким образом, это карбоновая кислота. В правой части структуры находится метильная группа -CH3(метильная группа — CH), которая представляет собой метильную группу.
Как видите, это очень маленькая и простая молекула. Благодаря группе -COOH существует постоянный дипольный момент, который также позволяет уксусной кислоте образовывать две последовательные водородные связи.
Именно эти мосты ориентируют СН пространственно3Молекулы UNOH образуют димеры в жидком (и газообразном) состоянии.
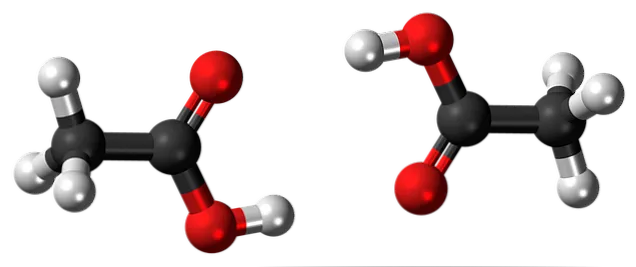
На изображении выше вы можете видеть, как две молекулы расположены таким образом, что образуют две водородные связи (O-H-O и O-H-O). Для того чтобы уксусная кислота испарилась, ей необходимо придать достаточно энергии для разрушения этих взаимодействий. Поэтому уксусная кислота — это жидкость с более высокой температурой кипения, чем вода (около 118°C).
ОттоХроматка и ГенрихЭбнер (1949) разработали резервуар с перемешиванием и подачей воздуха для аэробной ферментации для производства уксуса. Этот прибор до сих пор используется с некоторыми изменениями.
Производство уксусной кислоты путём карбонилирования метанола. Анализ существующих промышленных методов получения

Шахобиддинова, Н.Н. Получение уксусной кислоты карбонилированием метанола. Анализ существующих методов промышленного производства / Н.Н. Шахобиддинова, Д.А. Эргашева. — Текст: прямой // Молодые ученые. -2020.-№ 7 (297). -С. 1-5. -URL: https://moluch.ru/archive/297/67416/ (дата обращения: 15.06.2022).
Карбонилирование — это химическая реакция, в результате которой карбонильная группа C=O образуется при взаимодействии с монооксидом углерода. Для проведения этих реакций обычно используется гомогенный катализ и высокое давление.
Реакции карбонилирования также включают карбонилирование, окислительное и восстановительное карбонилирование. Гидрокарбонилирование включает гидроформилирование и гидроформилирование. 1
Ключевые слова: уксусная кислота, карбонилирование, метанол, общая характеристика производства, технологическая схема, процесс, катализ.
Сегодня карбонилирование является одним из ключевых направлений в гомогенном катализе металлокомплексов в химической промышленности. При введении карбонильных групп в молекулу могут образовываться различные классы органических соединений, включая альдегиды, кетоны, карбоновые кислоты и их производные, а также карбонаты. Преимуществами монооксида углерода в качестве реагента для реакций карбонилирования являются его реакционная способность, низкая стоимость и доступность благодаря наличию свободных пар электронов на атомах углерода. Процесс карбонилирования является более экономичным способом получения карбонильных соединений.
Уксусная кислота — важный продукт, используемый в химической промышленности, мировой спрос на который составляет около 9 миллионов тонн в год. Основными областями применения этого химического вещества являются приготовление ступенчатых ацетатов, дезинфицирующих средств, органических смесей и органических растворителей, а также производство фармацевтических препаратов, ацетата целлюлозы, парфюмерии и синтетических волокон.
Исследования рынка синтетической уксусной кислоты выявили значительный разрыв между спросом и предложением. Производство уксусной кислоты является глобальной проблемой, однако последние данные свидетельствуют о том, что производственные мощности во всем мире сокращаются. Поэтому производство синтетической уксусной кислоты необходимо расширять за счет более эффективных методов, таких как карбонилирование метанола.
Первый коммерчески доступный процесс карбонизации метанола с использованием кобальтовых катализаторов был разработан немецкой химической компанией BASF в 1963 году; в 1968 году был открыт катализатор Rhodes (CIS-RH(CO)2I2-), который в большинстве случаев может эффективно работать при более низких давлениях Он доступен По -Продуктам. Первые установки с использованием этого катализатора были произведены американской химической компанией Monsanto Company в 1970 году, после чего катализируемый Родсом метаноловый карбофос стал доминирующим методом производства кислоты. В конце 1990-х годов компания BP Chemicals выпустила на рынок катализатор Cativa (IR(CO)2I2-). Этот процесс, в котором используется катализатор цвета радуги, является более экологичным, более эффективным и в значительной степени заменил процесс Monsanto на том же производственном предприятии2. Однако в настоящее время на большинстве производств используются родионовские катализаторы, несмотря на их высокую селективность. высокой стоимости катализаторов Cativa.
Похожие статьи
Разработка эффективных полифункциональных катализаторов.
Однако использование всадников связано с некоторыми нежелательными процессами. В результате гидроксид алюминия был переварен с помощью уксусной кислоты. При разработке новых каталитических систем были выдвинуты теоретические положения и примеры.
Некоторые предпосылки подбора катализаторов синтеза пиррола.
Очевидно, что для такого процесса катализатор должен быть многофункциональным (иметь
Увеличение каталитических свойств оксида алюминия при обработке уксусной кислотой
Катализаторы, содержащие оксид хрома (III) в количестве 3-5%. В сочетании с уксусной кислотой.
Создание селективного катализатора для синтеза метанола
Хорошо известно, что совершенствование процесса производства метанола, создание пилотных установок и качество коммерческих продуктов зависит от ряда представлений об активности, селективности и термостабильности используемого катализатора.
Кинетика алкилирования этилбензола метанолом на.
Катализатор восстанавливают водородом, подаваемым со скоростью 40 мл/мин, до температуры 5000 С в течение 3 часов. Перед загрузкой катализатора в реактор его смешивали с инертной керамической добавкой. Смесь этилбензола и метанола нагревали до 1200 С и подавали в реактор.
Значение и получение терефталевой кислоты | Статья в сборнике.
Процесс производства органической кислоты (терефталевой кислоты), см. ниже.
При высоких концентрациях вода оказывает разрушающее воздействие на катализатор. Присутствие ионов марганца повышает стабильность катализатора.
Получение сложных эфиров и эфирных масел | Статья в журнале.
Уксусная кислота, кислоты, специальные нагрузки, повышение температуры, волокна, реакционные растворители, реакционная масса.
Для облегчения процесса гидролиза растительный материал подвергается предварительной обработке. Таким образом, при смешивании уксусной кислоты и пероксида.
Усовершенствование процесса получения цианистого натрия
Циановая кислота также производится каталитическим способом из формамида.
Катализатор состава помещается в середину, в платиновую трофейную сетку.
Этот вариант был выбран для улучшения процесса производства синильной кислоты.
Изучение физико-химических аспектов деструкции высококипящих.
Технические гликолитические исследования показали, что среди продуктов разложения, наряду с признанными низкокипящими продуктами (перекись водорода, формальдегид, ацетон, ANT, уксусная кислота и гидроксиды).
Разработка катализаторов для синтеза N-винилморфолина
Была разработана каталитическая система для реакции ацетилена с морфолином, в результате чего была получена матрица активированного угля с нанодобавками и измерен исходный размер активированного угля.
Разбавленные спиртовые растворы, зараженные ацетобактером и хранящиеся в теплом и проветриваемом месте, превращаются в уксус в течение нескольких месяцев. Промышленные методы изготовления уксуса ускоряют этот процесс, улучшая снабжение бактерий кислородом.
Применение
Уксусная кислота широко используется в различных отраслях промышленности.
- в фармацевтике – входит в состав лекарственных препаратов;
- в химической промышленности – используется для производства ацетона, красителей, ацетилцеллюлозы;
- в пищевой промышленности – применяется для консервации и вкуса;
- в лёгкой промышленности – используется для закрепления краски на ткани.
Уксусная кислота добавляет E260 Продукты питания.

Рисунок 3: Использование уксусной кислоты.








