После этого на металле появлялись окислы, препятствующие выработке энергии. Чтобы удалить этот окисел, конструкцию нужно было разобрать и протереть металл. А куски кожи приходилось время от времени смачивать соленой водой.
Источник эдс. идеальный и реальный источники
Электричество давно известно как источник энергии, поскольку сама природа производит его в больших количествах. Типичными примерами являются молния и электрические коньки. Несмотря на такую близость к человеку, использование этой энергии стало возможным только в середине 17 века. Мэр Магдебурга Отто фон Герике создал машину, которая позволяла генерировать статические заряды. В середине 18 века голландский ученый Питер фон Мушенбрук создал первый в мире электрический конденсатор, названный Лейденской бутылкой, в университете, где он работал.
Эра настоящих открытий в области электричества, вероятно, началась с работ Луиджи Гальвани и Алессандро Вольта, которые изучали образование токов в мышцах и в так называемых гальванических элементах, соответственно. Дальнейшие исследования открыли нам глаза на взаимосвязь между электричеством и магнетизмом и на различные очень полезные явления (например, электромагнитную индукцию). Без них невозможно было бы представить нашу сегодняшнюю жизнь.
Однако мы не занимаемся магнитными явлениями, а сосредоточимся исключительно на электрических. Давайте теперь рассмотрим, как вырабатывается электричество в гальванической батарее и что она собой представляет.

Каждая маркировка источника питания определяет принцип его работы. В обычных условиях энергия вырабатывается в результате взаимодействия компонентов.
- Механический тип. В результате взаимодействия деталей механизма, возникает трение. Благодаря такому явлению, возникает статическое электричество, преобразуемое в ток.
- Механические конструкции работают посредством образования последовательно движущихся заряженных частиц. Явление возникает благодаря взаимодействию химического элемента с электролитом. Заряженные частицы покидают структуру кристаллической решётки металла, входя в состав проводящей жидкости.
- Солнечные батареи (световые источники) работают за счет выбивания заряженных частиц из диэлектрической (кремниевой) основы под воздействием светового потока. Благодаря этому возникает постоянное напряжение.
- Тепловые. Как правило, это 2 последовательно соединенных металлических основания. Одна часть нагревается, а вторая остается охлажденной. При изменении температурного режима возникает разница температур, в результате чего происходит движение заряженных частиц.
Важно! Изменения в структуре вещества могут иметь необратимые последствия, и это происходит при работе устройства.
Конструкция
Конструкция элемента влияет на то, как он работает. Каждый источник питания имеет определенную конструкцию.
Простейшая бытовая батарейка состоит из металлического корпуса, внутри которого находится щелочной носитель. Дополнительным элементом является свинцовая пластина, из которой изготовлены катод и анод.
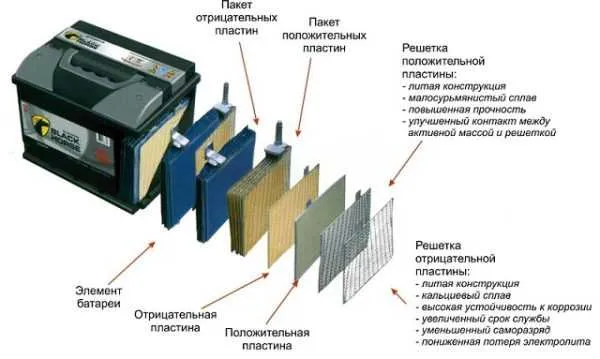
Батареи.
Стандартные бытовые батареи, включая батареи с сухими элементами, имеют металлический корпус с прикрепленным к нему стержнем катодного аккумулятора. Оставшееся пространство заполняется солевым электролитом.
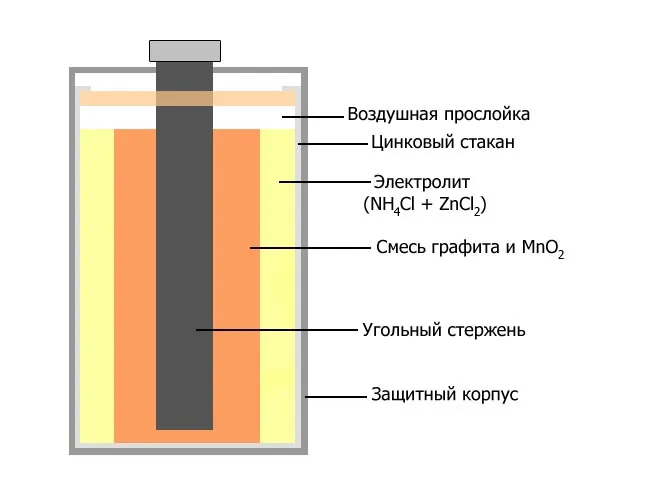
Аккумулятор.
Теплообменники представляют собой устройства, состоящие из храпового или металлического каркаса.
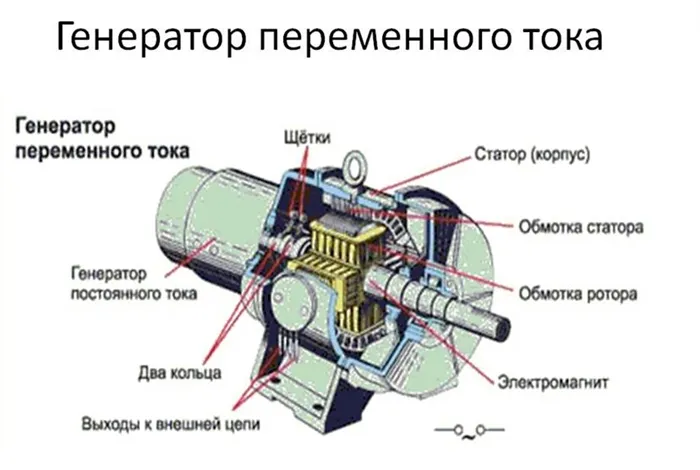
Механический принцип работы устройства.
тепловая электростанция, уже включенная в схему. Он представляет собой обычную рамку, установленную на диэлектрическом основании. Конструкция обычно подключается к измерительному прибору, например, амперметру. Источником тепла является пламя или внешний электрический импульс.

Тепловые устройства
Важно: Такие структуры помогают понять, как именно генерируется энергия, а затем преобразуется в ток. Варианты каждой структуры обычно заключены в специальный диэлектрический корпус.
В щелочных батареях в качестве электролита используется пастообразный щелочной раствор гидроксида калия. Цинковые аноды заменяются цинковым порошком, что увеличивает выход тока и время работы. Эти клетки служат в 1,5 раза дольше, чем солевые клетки.
Виды источников электрического тока
Источники питания выпускаются следующих типов.
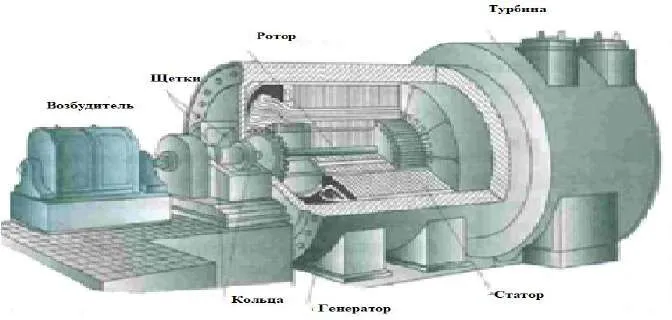
Эти источники преобразуют механическую энергию в электрическую. Преобразование происходит в специальных устройствах, таких как генераторы. Основными генераторами являются турбогенераторы, где электродвигатель приводится в движение потоком газа или пара, и водородные генераторы, которые преобразуют энергию падающей воды в электричество. Механические преобразователи вырабатывают большую часть электроэнергии на планете.

Тепловые источники
Здесь тепловая энергия преобразуется в электричество. Электрический ток генерируется за счет разницы температур между двумя парами соприкасающихся металлов или полупроводников (термопары). В этом случае заряженные частицы перемещаются из нагретой области в холодную. Величина тока напрямую зависит от разницы температур. Чем больше разница температур, тем больше ток. Термопары на основе полупроводников можно использовать для создания источников питания, поскольку они обеспечивают в 1000 раз большую теплоотдачу, чем биметаллические термопары. Металлические термопары используются только для измерения температуры.
В настоящее время разрабатываются новые элементы, основанные на преобразовании тепла, выделяемого при спонтанном распаде радиоизотопов. Эти элементы называются радиоизотопными термоэлектрическими генераторами. В хорошо испытанном генераторе космического аппарата используется изотоп плутоний-238. Он обеспечивает мощность 470 Вт при напряжении 30 В. Период полураспада этого изотопа составляет 87,7 лет, что обеспечивает генератору очень долгий срок службы. Теплообменник с электричеством представляет собой биметаллическую термопару.
Световые источники
С развитием физики полупроводников во второй половине 20-го века появился новый источник энергии: солнечные батареи, в которых световая энергия преобразуется в электричество. Они используют свойства полупроводников для получения напряжения при воздействии светового потока. В частности, кремниевые полупроводники обладают таким эффектом. Однако выход этих клеток не превышает 15%. Солнечные батареи стали неотъемлемой частью космической промышленности и начинают использоваться в повседневной жизни. Цена на эти источники энергии постоянно снижается, но остается очень высокой: около 100 рублей за ватт электроэнергии.

Термические варианты не работают, если они основаны на одном типе металла. При отсутствии источника тепла появление движущихся частиц исключено.
Регулируемые источники
Регулируемый источник состоит из следующих элементов

- понижающий трансформатор;
- выпрямитель;
- сглаживающий фильтр (устраняет пульсации);
- стабилизатор постоянного напряжения.
Регуляторы постоянного напряжения — это интегральные схемы, которые поддерживают выходное напряжение на одном уровне независимо от изменения входного напряжения.
колебания, вызванные изменениями напряжения сети, тока нагрузки или изменениями температуры. Агрегаты с такими стабилизаторами называются регулируемыми.
Сегодня широко распространены импульсные источники питания, которые состоят из следующих компонентов
- входной выпрямитель;
- инвертор;
- понижающий высокочастотный трансформатор;
- выходной выпрямитель.
Инвертор преобразует предварительно выпрямленный ток в переменный, но на значительно более высокой частоте (до 10-15 кГц). На этой частоте размеры трансформатора и потери значительно уменьшаются. Инвертор состоит из базового транзистора, управляемого микросхемой.
Тот же принцип применяется к сварочным инверторам, что объясняет их компактную форму.
Существуют различные стабилизированные интегральные схемы с разными характеристиками. Например, LM317 имеет номинальный ток до 1,5 А и регулирует выходное напряжение. Более мощным контроллером является LM350.
Вторичный химический источник — ток
Вторичный химический источник энергии является многоразовым — аккумулятор. Подъем батареи действует как ее падение во время разряда и заряда. Наиболее распространенными являются свинцовые (кислотные) и железо-никелевые (щелочные) аккумуляторы.
Вторичные химические источники энергии, работающие на основе использования обратимых электрохимических систем. Обратимые электрохимические системы — это системы, которые могут преобразовывать вещество, образующееся при разряде, в исходное активное вещество.
Вторичные химические источники питания являются многоразовыми. Батареи. Подъем батареи во время разряда действует как спад во время зарядки.
Относится к первичным и вторичным химическим источникам питания. Определяет требования безопасности при проектировании источников питания.
Антиэлемент — это вторичный химический источник питания, практически не имеющий полезной емкости и используемый для предотвращения интеграции в цепь батареи для регулирования напряжения батареи.
Настоящий стандарт распространяется на первичные и вторичные химические источники питания.
Стартерные свинцово-кислотные батареи являются вторичными химическими источниками энергии. Активные компоненты, входящие в их состав, являются многоразовыми.
Свинцово-кислотные батареи являются самыми популярными из всех вторичных химических источников энергии. Различные электрические параметры для разных целей и их характеристики в основном обусловлены различиями в технологии и конструкции электродных пластин. Наиболее распространенным типом стартерной батареи является пастеризационная батарея, которая и является предметом данной лабораторной работы.
Группа щелочных батарей с электродами из оксида никеля состоит из трех систем вторичного химического питания: никель-железо (сокращенно HJK), никель-кадмий (сокращенно NK) и никель-цинк. Последние в настоящее время не используются, в основном потому, что имеют ряд существенных недостатков, таких как короткий срок службы (менее 200 циклов) и высокий саморазряд (до 90% в месяц). Однако никель-цинковые батареи имеют высокую плотность энергии — 60 Вт-ч/кг, и поэтому являются перспективными.
Свинцово-кислотные батареи являются наиболее распространенным вторичным химическим источником энергии. В зависимости от назначения, их разнообразие электрических и функциональных параметров обеспечивается в основном различиями в технологии и конструкции электродных пластин.
Таким образом, один и тот же электрод химического источника вторичного тока может быть как анодом, так и катодом, в зависимости от того, заряжается или разряжается источник. Поэтому правильное использование терминов «подъем» и «спад» при исследовании вторичного ЦИТ требует знания природы процессов, происходящих на конкретном электроде во время зарядки и разрядки источника, предполагая, что термин «подъем» соответствует окислению. Термин катод в процессах и процессах восстановления.
В отличие от простых (первичных) гальванических батарей (см. 8.4), аккумуляторы являются вторичными химическими источниками энергии.
Прохождение электричества от электролитического элемента вызывает специфические изменения в элементе. Если происходящие электрохимические процессы обратимы, то электрическая работа может быть вновь получена из накопленной химической энергии. Такие обратимые элементы называются аккумуляторными батареями или вторичными химическими источниками.
Химические источники
Химические источники энергии, пожалуй, представляют наибольший интерес для пользователей. Они отличаются портативными размерами и принципом окислительно-восстановительных реакций. Один из кабелей обычно называется Ance (Плюс), а другой Descent (Минус). Первый окисляется, а второй восстанавливается в веществе. Пространство между электродами заполнено перегородками электролит — раствор.
Сегодня производство может предложить различные типы непрерывных химических генераторов. Основные из них перечислены в таблице:.
| Тип | Напряжение на выводах, В | Ёмкость, мАч | Градиент температур, °С |
| Солевый | 1,5 | 1000 — 1100 | -20 — 60 |
| Щелочной | 1,5 | 2400 — 2500 | -30 — 60 |
| Литий-тионилхлоридный | 3,3 — 3,6 | 2000 — 2100 | -55 — 85 |
| Литий-диоксидмарганцевый | 3 | 1500 — 1600 | -20 — 85 |
| Литий-диоксидсерный | 2,6 — 2,9 | 800 — 900 | -55 — 70 |
Химические источники имеют специфические характеристики.
- Напряжение без подключения нагрузки.
- Ёмкость — величина, зависящая от выработки тока относящейся к единице объёма.
- Мощность.
- Ток саморазряда.
Потеря емкости вызвана не только подключением нагрузки, но и химическими реакциями, происходящими в спокойном состоянии клеток. Из-за низкой мощности эти источники не используются в качестве источников притяжения. Для этой цели используются никель-кадмиевые и никель-сидирусовые элементы. Спуск производится из Nio, а подъем — из смеси кадмия и железа. Во время процесса снятия заряда электролит аккумулятора не испаряется. Происходящую реакцию можно описать следующим образом: 2Ni(OOH) + CD + 2 H2O = 2 Ni(OH)2 + CD(OH)2.
Щелочные батареи называют перезаряжаемыми никель-кадмиевыми и никель-гидридными аккумуляторами. Они используют гидроксид калия. Однако наиболее популярными являются свинцово-кислотные батареи, в которых электролитом является серная кислота.
В отчетах об источниках энергии часто упоминаются сахарные батареи SO Cole. Он работает на сахарозе и производит только воду. Поскольку оригинал все еще находится в стадии разработки, его возможности неизвестны.
Для производства электроэнергии необходимо выбрать источник энергии, соответствующий потребностям данного приложения. Существует несколько вариантов таких устройств, каждый из которых имеет определенную структуру, принцип работы и индивидуальные технические показатели.
Применение
Реальные генераторы имеют различные ограничения с различными нелинейными зависимостями (по выходному напряжению) от внешних условий. Например, генераторы реального тока вырабатывают мощность только в определенном диапазоне напряжений, но их верхние пределы зависят от напряжения питания источника. Поэтому фактический источник энергии имеет ограничение по грузоподъемности.
Источники питания широко используются в аналоговых схемах. Для питания измерительных мостов, в частности, уровня дифференциальных усилителей операционных усилителей.
Концепция генератора тока используется для представления реального электронного компонента в виде эквивалентной схемы. Для учета активных данных вставлена эквивалентная схема, содержащая управляемый осциллятор.
Вторичный химический источник энергии является многоразовым — аккумулятор. Подъем батареи действует как ее падение во время разряда и заряда. Наиболее распространенными являются свинцовые (кислотные) и железо-никелевые (щелочные) аккумуляторы.
Химические источники

Химические источники энергии, пожалуй, представляют наибольший интерес для пользователей. Они отличаются портативными размерами и принципом окислительно-восстановительных реакций. Один из кабелей обычно называется Ance (Плюс), а другой Descent (Минус). Первый окисляется, а второй восстанавливается в веществе. Пространство между электродами заполнено перегородками электролит — раствор.
Сегодня производство может предложить различные типы непрерывных химических генераторов. Основные из них можно привести в таблице:.
| Тип | Напряжение на выводах, В | Ёмкость, мАч | Градиент температур, °С |
| Солевый | 1,5 | 1000 — 1100 | -20 — 60 |
| Щелочной | 1,5 | 2400 — 2500 | -30 — 60 |
| Литий-тионилхлоридный | 3,3 — 3,6 | 2000 — 2100 | -55 — 85 |
| Литий-диоксидмарганцевый | 3 | 1500 — 1600 | -20 — 85 |
| Литий-диоксидсерный | 2,6 — 2,9 | 800 — 900 | -55 — 70 |
Возвышение этих источников состоит из лития, который имеет высокий отрицательный потенциал по сравнению с другими проводниками. Такие источники обеспечивают нагрузку энергией в течение длительного времени. Лучшими из них являются литий-тион-хлоридные элементы (Li/SoCL2).
Химические источники обладают специфическими свойствами.
- Напряжение без подключения нагрузки.
- Ёмкость — величина, зависящая от выработки тока относящейся к единице объёма.
- Мощность.
- Ток саморазряда.
Потеря емкости вызвана не только подключением нагрузки, но и химическими реакциями, происходящими в спокойном состоянии клеток. Из-за низкой мощности эти источники не используются в качестве источников притяжения. Для этой цели используются никель-кадмиевые и никель-сидирусовые элементы. Спуск производится из Nio, а подъем — из смеси кадмия и железа. Во время процесса снятия заряда электролит аккумулятора не испаряется. Происходящую реакцию можно описать следующим образом: 2Ni(OOH) + CD + 2 H2O = 2 Ni(OH)2 + CD(OH)2.

Щелочные батареи называют перезаряжаемыми никель-кадмиевыми и никель-гидридными аккумуляторами. Они используют гидроксид калия. Однако наиболее популярными являются свинцово-кислотные батареи, в которых электролитом является серная кислота.
В отчетах об источниках энергии часто упоминаются сахарные батареи SO Cole. Он работает на сахарозе и производит только воду. Поскольку оригинал все еще находится в стадии разработки, его возможности неизвестны.